
Plin je agregatno stanje tvari u kojem se molekule slobodno kreću, šire se kako bi ispunile raspoloživi prostor i snažno reagiraju na promjene tlaka, zapremine i temperature. Ovaj osnovni pojam važan je u industrijskoj primjeni jer se plinovi ne tretiraju kao tekućine ili kruti materijali. U sustavima komprimiranog zraka, pneumatskim aktuatorima, procesnim posudama, spremnicima za plin i opremi za izgaranje, mala promjena temperature ili zapremine može promijeniti tlak, protok, gustoću i sigurnosne zahtjeve. Razumijevanje ponašanja plinova pomaže inženjerima da ispravno dimenzioniraju komponente, izbjegnu nestabilan rad i prepoznaju kada jednostavne pretpostavke o idealnom plinu više nisu dovoljne.
Za industrijske čitatelje najpraktičnija je poanta jednostavna: plin je koristan jer se može komprimirati, proširiti i lako provoditi kroz cijevi i ventile, ali te iste osobine čine ga osjetljivim na gubitak tlaka, toplinu, curenje, kontaminaciju i nesigurne uvjete skladištenja. Pouzdan plinski sustav ne projektira se samo na temelju tlaka. Također uzima u obzir temperaturu, volumen, sastav plina, vlagu, potražnju protoka, kapacitet regulatora i radno okruženje.
Sadržaj
- Što definira plin kao agregatno stanje tvari?
- Zašto je ponašanje plina važno u industrijskim primjenama?
- Koja svojstva plinova bi inženjeri trebali prvo razumjeti?
- Kako zakoni o plinovima pomažu predvidjeti ponašanje industrijskih plinova?
- Koje se vrste plinova obično koriste u industriji?
- Koje uobičajene pogreške uzrokuju probleme u plinskom sustavu?
- Praktična kontrolna lista za plinske i pneumatske sustave
- Često postavljana pitanja o osnovnim konceptima plina
- Reference
Što definira plin kao agregatno stanje tvari?
Plin nema fiksni oblik ni fiksni volumen. Širi se dok ne ispuni spremnik ili dostupnu mrežu cjevovoda. U usporedbi sa čvrstim i tekućim tvarima, molekule plina su znatno udaljenije, pa tlak može značajno smanjiti volumen. Zato komprimirani zrak može pohranjivati energiju, zašto pneumatski cilindri mogu pomicati dijelove strojeva i zašto se plinski cilindri moraju smatrati opremom koja sadrži tlak, a ne jednostavnim spremnicima.
Na mikroskopskoj razini tlak plina proizlazi iz molekularnog gibanja. Pritisak plina detektira se kada molekule plina udare o zidove posude i stvore silu po jedinici površine.[1]. Ovo objašnjenje nije samo teorija iz učionice. To je razlog zašto su manometri, regulatori, sigurnosni ventili i spojevi otporni na tlak ključni u stvarnim uređajima.
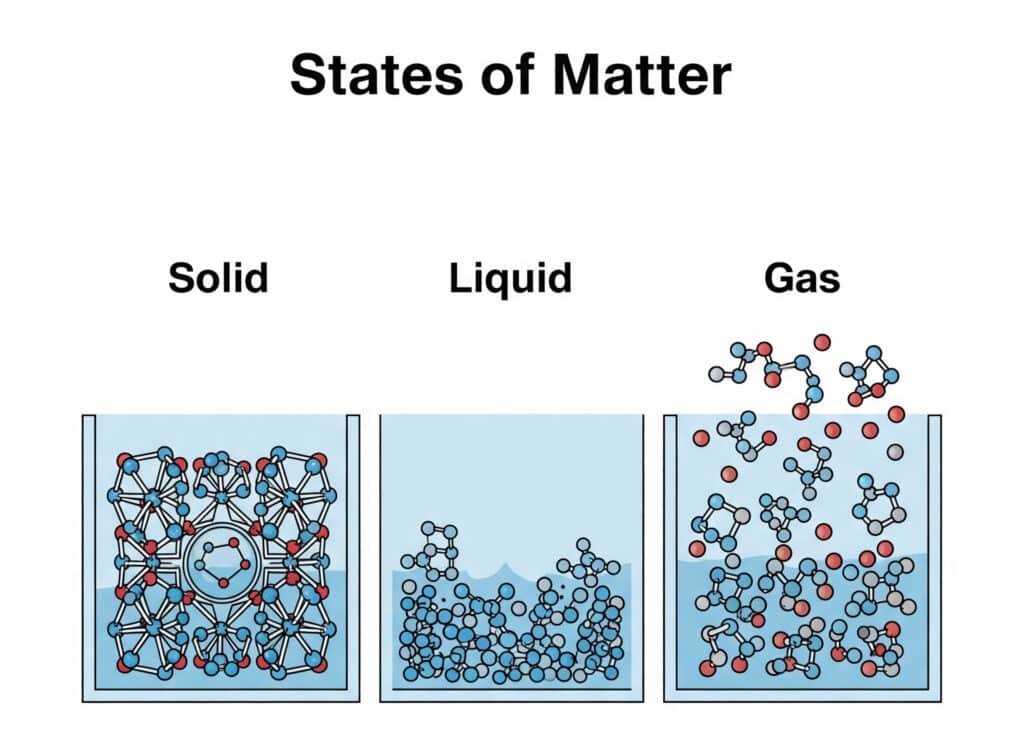
| Aggregacijsko stanje | Oblik | Svezak | Industrijsko značenje |
|---|---|---|---|
| Čvrst | Popravljeno | Skoro popravljeno | Koristi se za okvire, kućišta, alate i konstrukcijske dijelove gdje je dimenzionalna stabilnost važna. |
| Tekući | Poprimi oblik spremnika | Skoro popravljeno | Koristi se u hidraulici, hlađenju, podmazivanju i prijenosu kemikalija gdje je važna niska kompresibilnost. |
| plin | Poprimi oblik spremnika | Lako se širi ili skuplja | Koristi se u pneumatskom pokretu, ispiranju, zaštitnom opuhivanju, izgaranju, hlađenju, sušenju i skladištenju pod tlakom. |
Zašto je ponašanje plina važno u industrijskim primjenama?
Ponašanje industrijskih plinova je važno jer plinski sustavi rijetko rade pod jednim fiksnim uvjetom. Kompresori zagrijavaju zrak, dugi vodovi uzrokuju pad tlaka, ventili ograničavaju protok, cilindri ubrzavaju i usporavaju, a spremnici za pohranu mogu biti izloženi promjenjivim temperaturama okoline. Sustav koji u jednostavnoj računici funkcionira može postati nestabilan ako se zanemari stvarni tlak, temperatura, vlaga ili zahtjev za protokom.
U pneumatskoj automatizaciji ponašanje plina izravno utječe na silu izvršnog elementa, brzinu, prigušivanje, ponovljivost i potrošnju energije. Pneumatski cilindar može biti ocijenjen za određeni tlak, ali stvarni pokret ovisi o raspoloživom protoku na priključku, odzivu regulatora, promjeru cijevi, ograničenju na ispustu, trenju brtve i profilu opterećenja. Zato se dva stroja koja koriste isti nominalni tlak mogu ponašati vrlo različito.
U procesnim i skladišnim primjenama ponašanje plina utječe na sigurnost. Zagrijavanje plinskoga spremnika fiksnog volumena može povećati tlak. Brzo širenje može ohladiti plin i stvoriti rizik od kondenzacije ili smrzavanja. Plin obogaćen kisikom može pojačati izgaranje, dok inertni plinovi mogu istisnuti zrak za disanje u zatvorenim prostorima. Ispravno projektno pitanje nije samo “Koji nam je tlak potreban?” nego i “Što se događa ako se promijene temperatura, protok, sastav ili obuhvat?”
Koja svojstva plinova bi inženjeri trebali prvo razumjeti?
Najvažnija svojstva plina za industrijsku upotrebu su tlak, zapremina, temperatura, količina plina, gustoća, protok, sadržaj vlage i kemijsko ponašanje. Ta su svojstva međusobno povezana, pa promjena jednog često utječe na nekoliko drugih.
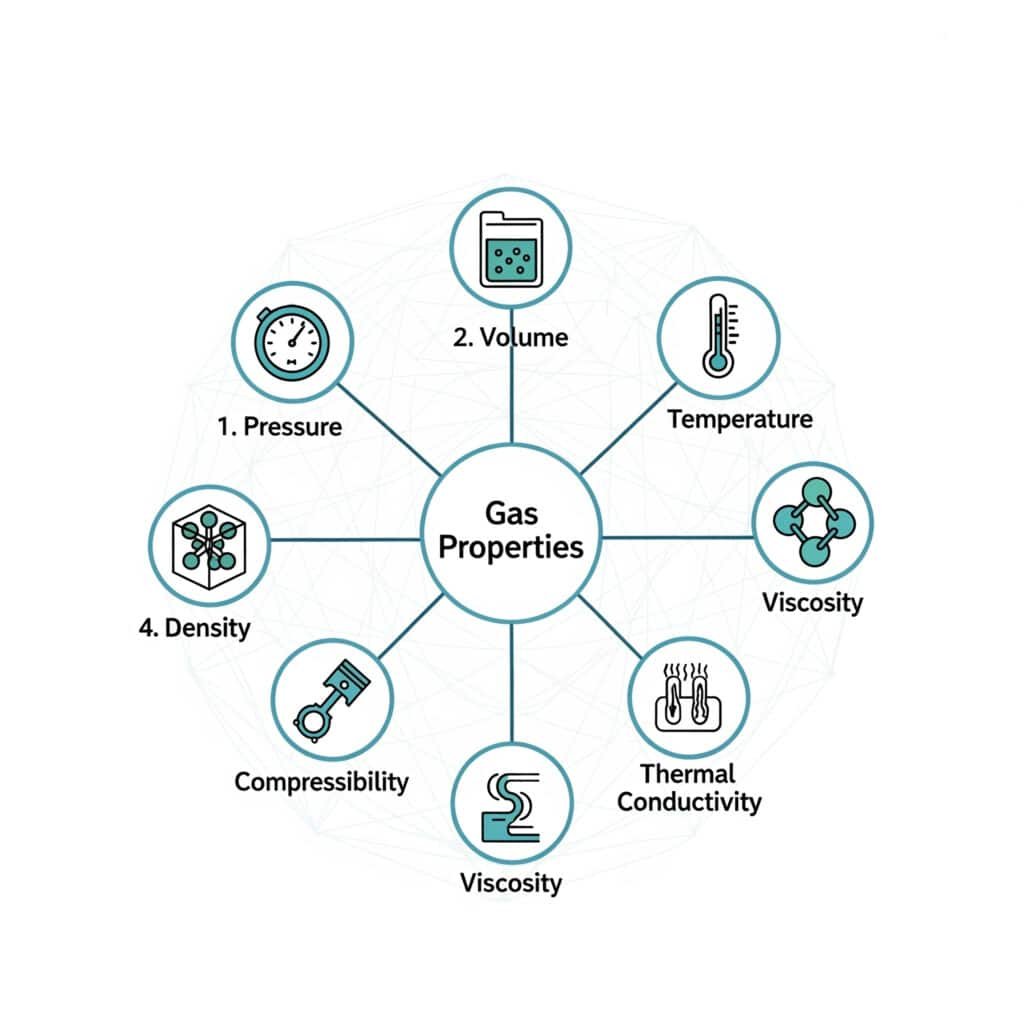
| Nekretnina | Što to znači | Zašto je to važno u industriji |
|---|---|---|
| Pritisak | Sila po jedinici površine koju stvaraju molekule plina i zadržavanje. | Određuje silu aktuatora, naprezanje posude, odabir regulatora i zaštitu od preopterećenja. |
| Svezak | Prostor dostupan za plin. | Utječe na kapacitet skladištenja, dimenzioniranje cilindara, potražnju za kompresorom i ponašanje pri ekspanziji. |
| Temperatura | Mjera povezana s molekularnom kinetičkom energijom. | Promjene tlaka, gustoće, viskoznosti, rizika od kondenzacije i materijalnih ograničenja. |
| Gustoća | Masa plina po jedinici zapremine. | Utjecaji na izračun protoka, ponašanje pri podizanju ili slijetanju, ventilaciju i mjerenje masenog protoka. |
| Protok | Količina plina koja se kreće po jedinici vremena. | Kontrolira brzinu aktuatora, učinkovitost ispiranja, rad brenera i kapacitet opskrbe procesa. |
| Sadržaj vlage | Vodena para nošena u plinu. | Može uzrokovati koroziju, zaleđivanje, zapinjanje ventila, loše podmazivanje i probleme sa senzorima. |
| Kemijsko ponašanje | Bilo da je plin inertan, oksidirajući, zapaljiv, toksičan, korozivan ili reaktivan. | Određuje kompatibilnost materijala, ventilaciju, detekciju, označavanje i postupke rada. |
Pritisak: više od očitanja na mjernom instrumentu
Tlak treba jasno navesti kao mjerni tlak ili apsolutni tlak. Mjerni tlak uspoređuje tlak sustava s atmosferskim tlakom, dok apsolutni tlak polazi od vakuuma. Mnoge formule za plinove zahtijevaju apsolutni tlak. Miješanje mjernog tlaka i apsolutnog tlaka čest je uzrok pogrešnog određivanja veličine i obmanjujućih izračuna.
Temperatura: skriveni čimbenik
Temperatura utječe na tlak, gustoću i ponašanje vlage. U cijevovodu komprimiranog zraka vrući zrak iz kompresora može zadržati više vodene pare. Kada se zrak hladi nizvodno, voda se može kondenzirati i dospjeti do ventila ili aktuatora. U zapečaćenom skladištu plina grijanje može povećati tlak čak i kad se ne dodaje dodatni plin.
Gustoća i protok: zašto “isti tlak” ne znači uvijek “iste performanse”
Gustoća plina mijenja se s tlakom i temperaturom. To utječe na količinu mase koja zapravo prolazi kroz ventil ili otvor. U pneumatskim sustavima manometar može pokazivati adekvatan tlak u mirovanju, no izvršni element i dalje se može kretati sporo ako dovodna cijev, ventil, spojka ili prigušnica ne mogu osigurati dovoljan protok pri dinamičkoj potražnji.
Kako zakoni o plinovima pomažu predvidjeti ponašanje industrijskih plinova?
Zakoni plinova pružaju praktičan okvir za predviđanje kako se plinovi ponašaju kada se promijene tlak, zapremina, temperatura ili količina plina. To su pojednostavljeni modeli, ali su korisni za početno dimenzioniranje, otklanjanje kvarova i razumijevanje uzroka i posljedica.
Zakon idealnog plina je najčešća polazna točka. Jednadžba stanja idealnog plina povezuje tlak, temperaturu, gustoću i plinski koeficijent.[2]. U molarskom obliku piše se PV = nRT, gdje je P apsolutni tlak, V volumen, n količina plina, R molarna plinska konstanta, a T apsolutna temperatura.
Pri uporabi SI jedinica, Molarna plinska konstanta prema NIST-u iznosi 8,314 462 618… J mol⁻¹ K⁻¹[3]. U praktičnom inženjerskom radu ispravan sustav jedinica jednako je važan kao i formula. Ispravna jednadžba s miješanim jedinicama i dalje može dati nesiguran odgovor.
| Zakon o plinovima ili proces | Jednostavan odnos | Korisni industrijski primjer | Praktična opreznost |
|---|---|---|---|
| Boyleov zakon | Pri konstantnoj temperaturi tlak i zapremina kreću se u suprotnim smjerovima. | Procjena kako kompresija mijenja tlak ili kapacitet pohrane. | Prava kompresija često zagrijava plin, pa temperatura možda neće ostati konstantna. |
| Charlesov zakon | Pri konstantnom tlaku zapremina se povećava s porastom apsolutne temperature. | Procjena širenja u procesima grijanja, sušenja i ventilacije. | Koristite apsolutnu temperaturu, a ne izravno Celzijus ili Fahrenheit. |
| Gay-Lussacov zakon | Pri konstantnom zapremini tlak raste s porastom apsolutne temperature. | Procjena porasta tlaka u zapečaćenim posudama izloženim toplini. | Nikada ne pretpostavljajte da je zatvoreni spremnik plina siguran samo zato što je početni tlak nizak. |
| Zakon o kombiniranom plinu | Pritisak, zapremina i temperatura mogu se povezati za fiksnu količinu plina. | Uspoređivanje stanja skladištenja ili procesa prije i nakon promjena temperature i tlaka. | Masovni curenje, kondenzacija i promjene faze mogu poništiti jednostavan model. |
| Stvarno ponašanje plina | Za stvarne plinove mogu biti potrebni korektivni faktori pri visokom tlaku, niskoj temperaturi ili u blizini fazne promjene. | Skladištenje pod visokim tlakom, specijalni plinovi, rashladni plinovi i procesni plinovi. | Koristite podatke dobavljača ili odgovarajuću jednadžbu stanja za kritične primjene. |
Gdje pretpostavke idealnog plina dobro funkcioniraju
Računanja idealnog plina često su dovoljna za obični zrak, dušik, kisik i slične plinove pri umjerenim tlakovima i temperaturama, kada je plin daleko od stanja kondenzacije ili kritičnih uvjeta. Korisna su za procjenu promjena zapremine, promjena tlaka, trendova gustoće i općeg pneumatskog ponašanja.
Gdje pretpostavke idealnog plina postaju rizične
Pretpostavke idealnog plina postaju manje pouzdane pri visokom tlaku, niskoj temperaturi, blizu tečnjaka ili kod plinova sa snažnim molekularnim interakcijama. U tim slučajevima inženjeri bi trebali koristiti podatke o stvarnom plinu, faktore kompresibilnosti, tehničke podatke dobavljača ili alate za simulaciju procesa. To je osobito važno za skladištenje pri visokom tlaku, rashladne krugove, kriogene plinske sustave i specijalne procesne plinove.
Koje se vrste plinova obično koriste u industriji?
Industrijski plinovi se odabiru prema funkciji, a ne samo prema dostupnosti. Plin se može odabrati zato što je inertan, reaktivan, oksidirajući, zapaljiv, suh, čist, jeftin, lako komprimiran ili kompatibilan s procesnim materijalom. Isti plin može biti siguran u jednom okruženju, a opasan u drugom.
| Kategorija plina | Uobičajeni primjeri | Glavne industrijske primjene | Ključni rizik za provjeru |
|---|---|---|---|
| Komprimirani zrak | Zrak za postrojenje, zrak za instrumente, osušeni zrak | Pneumatski cilindri, ventili, alati, odzračivanje, upravljački sustavi. | Vlažnost, ulje, pad tlaka, kontaminacija, nestabilan protok. |
| Neaktivni plinovi | dušik, argon, helij | Prekrivanje, pročišćavanje, zaštita pri zavarivanju, ispitivanje curenja. | Iskorištavanje kisika i gušenje u slabo prozračenim prostorima. |
| Oksidirajući plinovi | Kisik, kisikom obogaćene smjese | Gorenje, rezanje, medicinske i procesne primjene. | Povećana intenzitet vatre i zahtjevi za kompatibilnost materijala. |
| Goriva plinova | Prirodni plin, propan, vodik, aceton | Grijanje, rezanje, zavarivanje, izgaranje, energetski sustavi. | Požar, eksplozija, otkrivanje curenja, ventilacija, izvori paljenja. |
| Reaktivni ili toksični plinovi | Amonijak, klor, sumporov dioksid i drugi | Kemijska proizvodnja, klimatizacija, pročišćavanje vode, procesne reakcije. | Izloženost toksinima, korozija, hitni odgovor, kompatibilni materijali. |
| Specijalni plinovi | Kalibracijski plinovi, plinovi iznimno visoke čistoće, mješoviti plinovi | Instrumentacija, laboratoriji, procesi poluvodiča, kontrola kvalitete. | Čistoća, kontaminacija u tragovima, rukovanje cilindrom i dokumentacija. |
Komprimirani zrak zaslužuje posebnu pažnju jer je toliko uobičajen da ga timovi ponekad podcijene. Zrak izgleda bezopasno, ali komprimirani zrak sadrži pohranjenu energiju i može sadržavati vodu, uljnu maglicu, čestice i pulsacije tlaka. Za pneumatsku opremu kvaliteta zraka i protočni kapacitet često su jednako važni kao i nominalni tlak.
Gasni boce također zahtijevaju disciplinirano rukovanje. OSHA zahtijeva od poslodavaca da utvrde da su boce s komprimiranim plinovima pod njihovom kontrolom u sigurnom stanju, koliko se to može utvrditi vizualnim pregledom.[4]. Ovo podupire praktično pravilo: nikada ne smatrajte cilindar, regulator, crijevo ili ventil prihvatljivima samo zato što su prošli put bili uspješno korišteni.
Klasifikacija opasnosti također je važna. Plinovi pod tlakom označavaju se upozorenjima kao što su: sadrži plin pod tlakom i može eksplodirati ako se zagrije.[5]. Hladnjom rashlađeni plinovi predstavljaju poseban rizik jer vrlo niska temperatura može uzrokovati kriogeni opekline ili ozljede.
Koje uobičajene pogreške uzrokuju probleme u plinskom sustavu?
Mnogi kvarovi na plinskim sustavima ne nastaju zbog neznanja formule. Nastaju zbog primjene formule bez razumijevanja okolnih uvjeta. Najčešće su pogreške praktične, a ne teorijske.
- Korištenje manometarskog tlaka u formulama koje zahtijevaju apsolutni tlak. Ovo može iskriviti procjene gustoće, volumena i protoka.
- Pod pretpostavkom da je tlak jednak protoku. Sustav može pokazivati ispravan statički tlak, a istovremeno uskraćivati aktuatoru dovod tijekom kretanja.
- Zanemarivanje porasta temperature tijekom kompresije. Kompresijska toplina utječe na tlak, ponašanje vlage, vijek trajanja maziva i stanje brtve.
- Regulatori i ventili prevelike ili premale veličine. Regulator koji izgleda ispravno prema veličini priključka možda neće osigurati potreban protok pri potrebnom padu tlaka.
- Zaboravljanje vlage u komprimiranom zraku. Voda može korodirati dijelove, začepiti male prolaze, zalediti se na hladnim područjima i smanjiti pouzdanost pneumatskog sustava.
- Tretiranje svih plinova kao zraka. Kisik, vodik, amonijak, dušik, argon i CO₂ imaju različite opasnosti i zahtjeve kompatibilnosti.
- Ignoriranje ograničenja ispušnih plinova. Prigušivači, brzi ispušni ventili i male cijevi mogu promijeniti brzinu aktuatora i ponašanje prigušivanja.
- Preskakanje provjera curenja. Male curenja plina rasipaju energiju, smanjuju stabilnost tlaka i mogu stvoriti rizik od požara, toksičnosti ili gušenja, ovisno o plinu.
Praktična kontrolna lista za plinske i pneumatske sustave
Prije odabira komponenti ili otklanjanja kvarova na plinskom sustavu, najprije prikupite osnovne operativne informacije. Time se izbjegava čest problem odabira dijelova samo na temelju nominalnog tlaka.
- Identificirajte vrstu plina, čistoću, stanje vlažnosti i klasifikaciju opasnosti.
- Zabilježite tlak opskrbe, radni tlak, očekivani pad tlaka i navedite jesu li vrijednosti mjerni ili apsolutni.
- Definirajte minimalnu i maksimalnu radnu temperaturu, uključujući pokretanje, zaustavljanje i izlaganje okolišnim uvjetima.
- Procijenite potražnju protoka tijekom stvarne operacije, a ne samo tijekom stalnih radnih uvjeta.
- Provjerite duljinu cijevi, unutarnji promjer, priključke, prigušnike, regulatore, ventile i ograničenja.
- Potvrdite materijalsku kompatibilnost brtvila, maziva, metala, plastika i premaza.
- Provjerite može li se plin kondenzirati, pretvoriti u tekućinu, zalediti, reagirati ili kontaminirati proces.
- Potvrdite da su cilindri, posude, crijeva, regulatori i priključci ocijenjeni za stvarni tlak i rad sa plinom.
- Planirajte ventilaciju, otkrivanje curenja, označavanje, održavanje i hitni odgovor gdje je to potrebno.
- Za pneumatski pokret ispitati brzinu, silu, prigušivanje, ponovljivost i vrijeme oporavka pod stvarnim opterećenjem.
Kako se ovo primjenjuje na pneumatsku automatizaciju?
Pneumatska automatizacija koristi ponašanje plina na kontroliran način. Stlađeni zrak pohranjuje energiju, ventili usmjeravaju tu energiju, a izvršni elementi je pretvaraju u pokretanje. Osnovni koncept plina objašnjava zašto su pneumatski sustavi brzi, jednostavni i fleksibilni, ali i zašto su osjetljivi na kvalitetu zraka, curenje, pad tlaka i neujednačeno opskrbljivanje protokom.
Prilikom odabira pneumatskih komponenti započnite s potrebnom silom i brzinom, a zatim provjerite raspoloživu opskrbu zrakom. Veći cilindar može proizvesti veću silu, ali i potrošiti više zraka. Manji ventil može smanjiti troškove, ali može ograničiti brzinu. Duže cijevi mogu pojednostaviti raspored stroja, ali mogu odgoditi odziv. Dobar dizajn uravnotežuje tlak, protok, veličinu cilindra, kapacitet ventila, duljinu cijevi i zahtjeve za upravljanje.
Za timove za održavanje najbolji redoslijed otklanjanja kvarova obično je vizualni pregled, provjera tlaka, provjera curenja, provjera kvalitete zraka, provjera ograničenja protoka, a zamjenu komponenti vršiti tek kada dokazi upućuju na neispravan dio. Zamjena cilindara ili ventila bez provjere uvjeta opskrbe plinom često samo na kratko prikriva izvorni problem.
Često postavljana pitanja o osnovnim konceptima plina
Koja je osnovna koncepcija plina?
Plin je stanje tvari u kojem se molekule slobodno kreću, rasprostiru se kako bi ispunile raspoloživi prostor i značajno mijenjaju zapreminu pri promjenama tlaka ili temperature. To čini plin korisnim za kompresiju, protok, ispiranje i pneumatski pokret, ali također zahtijeva pažljivu kontrolu.
Zašto je plinove lakše komprimirati nego tekućine?
Plinove je lakše komprimirati jer su njihove molekule mnogo udaljenije od molekula tekućina. Pritisak može smanjiti prostor između molekula plina, dok tekućine imaju mnogo manje slobodnog prostora za smanjenje.
Zašto se tlak plina povećava kad temperatura raste?
Kada temperatura poraste, molekule plina se kreću s više energije. U fiksnom volumenu one se snažnije i češće sudaraju sa zidovima posude, pa tlak raste. To je važno za zapečaćene posude, boce i opremu izloženu toplini.
Je li komprimirani zrak isto što i industrijski plin?
Komprimirani zrak je jedna vrsta industrijskog opskrbivanja plinom, ali se ne ponašaju svi industrijski plinovi kao komprimirani zrak. Dušik, kisik, argon, vodik, amonijak, CO₂ i specijalne smjese imaju različite zahtjeve u pogledu sigurnosti, čistoće, kompatibilnosti materijala i rukovanja.
Koja je najčešća pogreška pri izračunima pneumatskog plina?
Najčešća pogreška je pretpostaviti da sam tlak određuje performanse. Pneumatske performanse također ovise o protočnom kapacitetu, promjeru cijevi, Cv ventila, odzivu regulatora, ograničenju ispušnog otvora, kvaliteti zraka i uvjetima opterećenja.
Kada bi se trebalo uzeti u obzir ponašanje idealnog plina?
Stvarno ponašanje plina treba uzeti u obzir pri visokom tlaku, niskoj temperaturi, blizu kondenzacije ili likvifikacije ili pri radu sa specijalnim plinovima. U tim slučajevima koristite podatke dobavljača, inženjerski softver ili odgovarajuće jednadžbe stanja umjesto da se oslanjate samo na zakon idealnog plina.
Zaključak
Osnovni koncept plina nije samo znanstvena definicija. To je praktičan inženjerski alat. Plinovi ispunjavaju raspoloživi prostor, komprimiraju se pod tlakom, šire se s temperaturom, prolaze kroz uska mjesta i stvaraju tlak molekularnim gibanjem. U industrijskim primjenama ta ponašanja utječu na brzinu izvođača, opterećenje kompresora, sigurnost skladištenja, čistoću plina, kompatibilnost materijala i stabilnost procesa. Najsigurniji i najpouzdaniji sustavi projektiraju se uzimajući u obzir tlak, volumen, temperaturu, protok, vrstu plina i radno okruženje zajedno.
Ako birate pneumatske cilindre, ventile, jedinice za pripremu zraka ili priključke za automatizacijski projekt, pripremite radni tlak, potrebnu silu, hod, brzinu ciklusa, kvalitetu zraka i radno okruženje prije usporedbe opcija. Ove informacije pomažu dobavljačima i inženjerima da preporuče komponente koje odgovaraju stvarnom ponašanju plina, a ne samo kataloškom nazivnom tlaku.
Reference
- NASA Glenn istraživački centar — Pritisak plina. Pristupljeno 2026-05-21. Uloga dokaza: mehanizam; Vrsta izvora: vladin. Podržava: Objašnjenje da tlak plina proizlazi iz sudara molekula plina sa stijenkama posude i stvaranja sile po jedinici površine. ↩
- NASA Glenn istraživački centar — Jednadžba stanja / Idealni plin. Pristupljeno 2026-05-21. Uloga dokaza: general_support; Vrsta izvora: vladin. Podržava: Upotrebu jednadžbe stanja idealnog plina za povezivanje tlaka, temperature, gustoće i plinske konstante. ↩
- NIST CODATA vrijednost: Molarni gasni koeficijent. Pristupljeno 2026-05-21. Uloga dokaza: statistički; Vrsta izvora: vladin. Podržava: navedenu SI vrijednost molarne plinske konstante koja se koristi u izračunima idealnog plina. ↩
- OSHA 29 CFR 1910.101 — Stlađeni plinovi, opći zahtjevi. Pristupljeno 2026-05-21. Uloga dokaza: general_support; Vrsta izvora: vladin. Podržava: Zahtjev da poslodavci utvrde jesu li komprimirani plinski cilindri pod njihovom kontrolom u sigurnom stanju, koliko to vizualni pregled može utvrditi. Napomena o opsegu: Ovaj izvor odražava zahtjeve američke OSHA-e i treba ga provjeriti u odnosu na lokalne propise za radna mjesta izvan SAD-a. ↩
- Kanadski centar za sigurnost i zdravlje na radu — Opasni proizvodi: upotreba piktograma plinskog bočca. Pristupljeno 2026-05-21. Uloga dokaza: general_support; Vrsta izvora: vladin. Podržava: Točku o komunikaciji opasnosti da plinovi pod tlakom mogu nositi upozorenja poput "sadrži plin pod tlakom i može eksplodirati ako se zagrije", uz zasebna upozorenja za rashlađene ukapljene plinove. ↩


