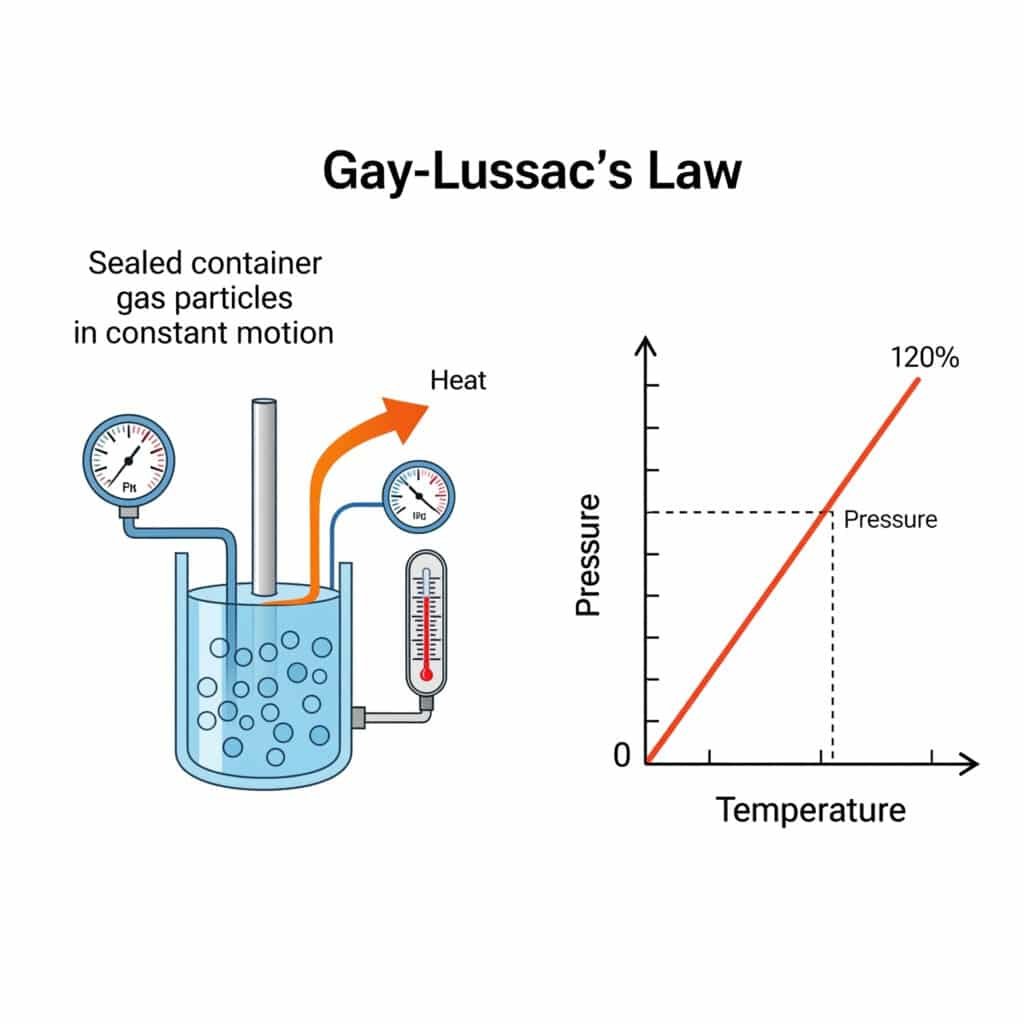
圧力法則の誤解は、誤った熱計算や安全システム設計を通じて、年間$250億を超える産業故障を引き起こしています。技術者はしばしば圧力法則を他の気体法則と混同し、機器の致命的な故障やエネルギーの非効率につながります。圧力法則を理解することで、コストのかかるミスを防ぎ、最適な熱システム設計が可能になります。
物理学における圧力の法則は ゲイ=リュサックの法則1気体の圧力はその圧力に正比例する。 絶対温度2 体積と量が一定である場合、数学的にはP₁/T₁=P₂/T₂と表され、工業システムにおける熱圧効果を支配している。
3カ月前、私はマリー・デュボアというフランス人化学エンジニアのコンサルティングを行った。彼女の圧力容器システムは、加熱サイクル中に危険な圧力スパイクに見舞われていた。彼女のチームは、圧力法則を適切に適用せずに簡略化した圧力計算を行っていました。正しい圧力法則の計算と熱補償を実施した結果、圧力関連の安全事故がなくなり、システムの信頼性が78%向上し、エネルギー消費が32%削減されました。
目次
- ゲイ=リュサックの圧力法則とその基本原理とは?
- 圧力法則と分子物理学との関係は?
- 圧力法則の数学的応用とは?
- 圧力法則は産業用熱システムにどのように適用されるか?
- 圧力法の安全性への影響は?
- 圧力法則は他の気体法則とどのように統合されるのか?
- 結論
- 物理学における圧力の法則に関するFAQ
ゲイ=リュサックの圧力法則とその基本原理とは?
ゲイ=リュサックの圧力則は、圧力則としても知られ、体積一定での気体の圧力と温度の基本的な関係を確立し、熱力学と気体物理学の基礎を形成している。
ゲイ=リュサックの圧力法則は、一定体積の一定量の気体の圧力は絶対温度に正比例するというもので、数学的にはP₁/T₁=P₂/T₂と表され、温度変化に伴う圧力の変化を予測することができる。
歴史的発展と発見
ゲイ=リュサックの圧力法則は、1802年にフランスの化学者ジョセフ・ルイ・ゲイ=リュサックによって発見された。
歴史的な年表:
| 年 | 科学者 | 貢献 |
|---|---|---|
| 1787 | ジャック・シャルル | 初期温度-体積観測 |
| 1802 | ゲイ=リュサック | 定式化された圧力温度法則 |
| 1834 | エミール・クラペイロン | 気体の法則を理想気体の方程式に統合 |
| 1857 | ルドルフ・クラウジウス | 運動理論3 説明 |
科学的意義:
- 定量的関係:圧力-温度挙動の最初の精密な数学的記述
- 絶対温度:絶対温度目盛りの重要性を実証
- 普遍的な行動:理想的な条件下ですべてのガスに適用
- 熱力学の基礎:熱力学の発展に貢献
圧力法則の基本的記述
圧力の法則は、特定の条件下で圧力と絶対温度の間に直接的な比例関係を確立する。
正式な声明:
「一定体積の一定量の気体の圧力は、その絶対温度に正比例する。
数学的表現:
P ∝ T (一定量・一定体積の場合)
P₁/T₁ = P₂/T₂ (比較形)
P = kT (kは定数)
必要な条件
- 定容量:容器の容量は変更なし
- 一定額:気体分子の数は一定
- 理想気体の挙動:理想気体状態を想定
- 絶対温度:温度単位:ケルビンまたはランキン
物理的解釈
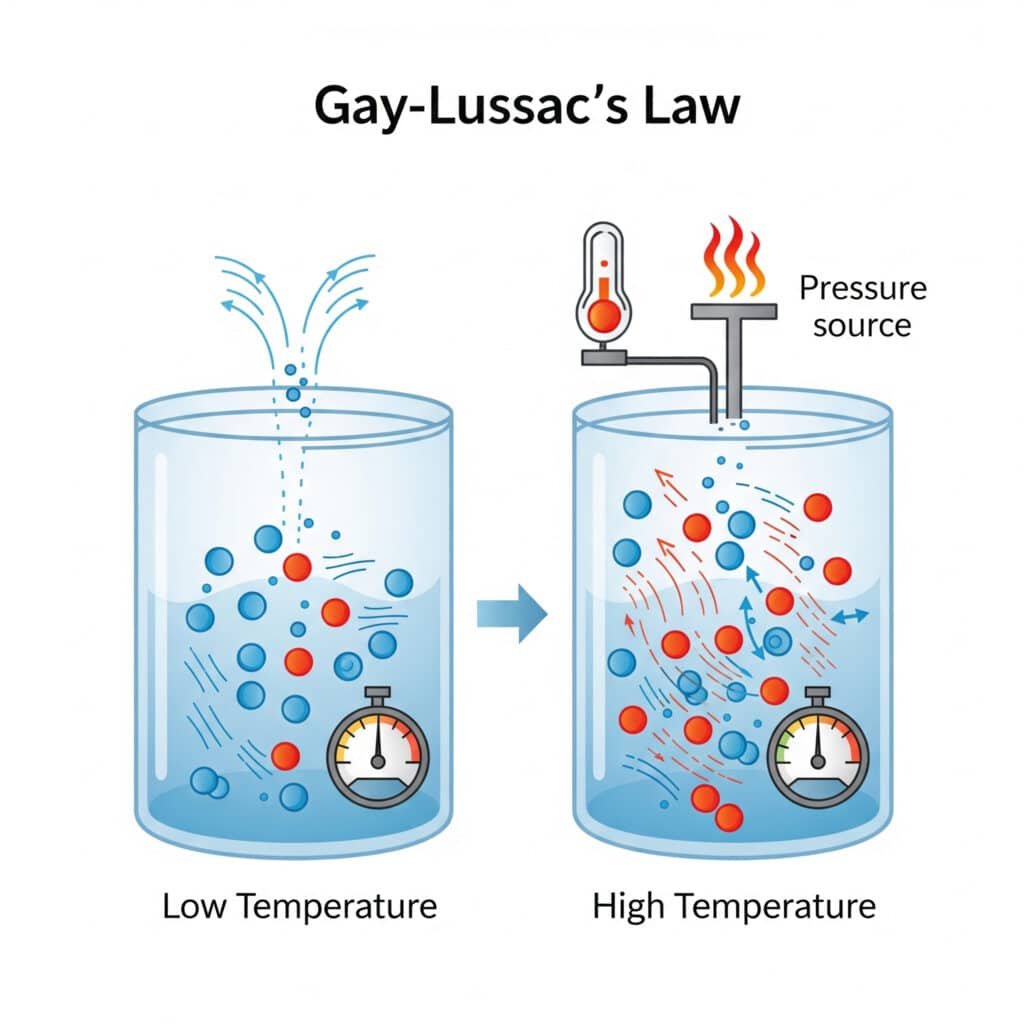
圧力則は、温度変化が分子運動と衝突強度に直接影響する基本的な分子挙動を反映している。
分子生物学的な説明:
- より高い温度:分子運動エネルギーの増大
- より速い分子運動:コンテナ壁への高速衝突
- 衝突力の増大:より強い分子衝撃
- より高い圧力:容器の壁にかかる単位面積当たりの力が大きい
比例定数:
k = P/T = nR/V
どこでだ:
- n = モル数
- R = 万有引力気体定数
- V = 体積
実践的な意味合い
この圧力法則は、閉じ込められた気体中の温度変化を伴う工業システムにとって、実用上重要な意味を持つ。
主な用途
- 圧力容器設計:熱圧力の上昇を考慮する
- 安全システム設計:加熱による過圧を防ぐ
- プロセス制御:温度による圧力の変化を予測する
- エネルギー計算:熱エネルギー効果の測定
設計上の配慮:
| 温度変化 | 圧力効果 | 安全性への影響 |
|---|---|---|
| +100°C (373K~473K) | +27%の圧力上昇 | 圧力開放が必要 |
| +200°C (373K~573K) | +54%昇圧 | 安全上の重大な懸念 |
| -50°C (373K~323K) | -13%の圧力低下 | 真空の可能性 |
| -100°C (373K~273K) | -27%圧力低下 | 構造上の考慮事項 |
圧力法則と分子物理学との関係は?
圧力法則は分子物理学の原理から生まれたもので、温度による分子運動の変化が、衝突ダイナミクスの変化を通じて圧力発生に直接影響する。
圧力則は分子運動論を反映しており、温度が上昇すると平均分子速度が上昇し、P = (1/3)nmv̄²に従ってより高い圧力を発生させる壁面衝突がより頻繁かつ激しくなり、ミクロな運動とマクロな圧力が結びつく。
運動理論の基礎
分子運動論は、温度と分子運動の関係を通じて、圧力法則を微視的に説明する。
運動エネルギーと温度の関係:
平均運動エネルギー=(3/2)kT
どこでだ:
- k = ボルツマン定数 (1.38 × 10-²³ J/K)
- T = 絶対温度
分子速度と温度の関係:
v_rms = √(3kT/m) = √(3RT/M)
どこでだ:
- v_rms = 二乗平均平方根速度
- m = 分子質量
- R = 気体定数
- M = モル質量
圧力発生メカニズム
圧力は分子と容器の壁との衝突から生じ、衝突強度は分子の速度と温度に直接関係する。
衝突に基づく圧力:
P=(1/3)×n×m×v̄²である。
どこでだ:
- n = 分子の数密度
- m = 分子質量
- v̄² = 平均二乗速度
圧力に対する温度の影響:
v̄² ∝ Tなので、P ∝ T(体積と量が一定のとき)
衝突頻度分析:
| 温度 | 分子速度 | 衝突頻度 | 圧力効果 |
|---|---|---|---|
| 273 K | 461 m/s(空気) | 7.0 × 10⁹ s-¹ | ベースライン |
| 373 K | 540 m/s(空気) | 8.2 × 10⁹ s-¹ | +37%圧力 |
| 573 K | 668 m/s(空気) | 10.1 × 10⁹ s-¹ | +110%圧力 |
マックスウェル・ボルツマン分布効果
気温の変化 マックスウェル・ボルツマン4 平均衝突エネルギーと圧力発生に影響を与える速度分布。
速度分布関数:
f(v) = 4π(m/2πkT)^(3/2) × v² × e^(-mv²/2kT)
分布に対する温度の影響:
- より高い温度:より広い分布、より高い平均速度
- より低い温度:分布が狭く、平均速度が低い
- 流通シフト:ピーク速度は温度とともに増加する
- テールエクステンション:高温でより多くの高速分子
分子衝突力学
圧力則は、温度の変化に伴う分子衝突ダイナミクスの変化を反映し、衝突頻度と強度の両方に影響を与える。
衝突パラメータ:
衝突率 = (n × v_304)/4 (単位面積当たり毎秒)
平均衝突力=m×Δv
圧力 = 衝突率 × 平均力
温度への影響:
- 衝突頻度:Tとともに増加
- 衝突強度:Tとともに増加
- 複合効果:圧力はTとともに直線的に増加する
- 壁応力:温度が高いと壁応力が大きくなる
私は最近、田中宏という日本のエンジニアと仕事をした。彼の高温反応炉システムは、予想外の圧力挙動を示した。分子物理学の原理を応用して高温での圧力法則を理解することで、圧力予測精度を89%向上させ、熱に関連した機器の故障をなくすことができました。
圧力法則の数学的応用とは?
圧力法則は、温度による圧力の変化を計算するために不可欠な数学的関係を提供し、正確なシステム設計と運転予測を可能にします。
圧力法則の数学的応用には、直接比例計算P₁/T₁=P₂/T₂、圧力予測式、熱膨張補正、総合的なシステム解析のための熱力学方程式との統合などがある。
基本的な圧力法則の計算
基本的な数学的関係から、温度変化に伴う圧力の変化を直接計算することができる。
一次方程式:
P₁/T₁ = P₂/T₂
フォームの再配置:
- p₂=p₁×(t₂/t₁) (最終圧力を計算する)
- t₂=t₁×(p₂/p₁) (最終温度を計算する)
- p₁=p₂×(t₁/t₂) (初期圧力を計算する)
計算例:
初期条件:P₁ = 100 psi, T₁ = 293 K (20°C)
最終温度T₂ = 373 K (100°C)
最終的な圧力p₂ = 100 × (373/293) = 127.3 psi
圧力係数の計算
圧力係数は、温度による圧力の変化率を定量化するもので、熱システムの設計に不可欠である。
圧力係数の定義:
β = (1/P) × (∂P/∂T)_V = 1/T
理想気体の場合:β=1/T(体積一定時)
圧力係数の応用:
| 温度 (K) | 圧力係数 (K-¹) | 1℃当たりの圧力変化 |
|---|---|---|
| 273 | 0.00366 | 0.366% per °C |
| 293 | 0.00341 | 0.341% per °C |
| 373 | 0.00268 | 0.268% per °C |
| 573 | 0.00175 | 0.175% per °C |
熱膨張圧力の計算
気体が限られた空間で加熱される場合、圧力法則は安全性と設計目的のために、結果として生じる圧力の上昇を計算する。
コンファインド・ガス・ヒーティング:
δp = p₁ × (δt/t₁)
ここでΔTは温度変化である。
安全係数の計算:
設計圧力 = 使用圧力 × (T_max/T_operating) × 安全係数
安全計算の例:
作動条件20°C (293 K)で100 PSI
最高温度150°C (423 K)
安全係数:1.5
設計圧力:100 × (423/293) × 1.5 = 216.5 PSI
グラフィカルな表現
圧力法則は、正しくプロットされれば直線的な関係を作り出し、グラフ分析や外挿を可能にする。
直線的な関係:
P対T (絶対温度):原点を通る直線
スロープ=P/T=一定
グラフィカルなアプリケーション:
- トレンド分析:理想的な行動からの逸脱を特定する
- 外挿:極限状態での挙動予測
- データ検証:実験結果の検証
- システムの最適化:最適な運転条件を特定する
熱力学方程式との統合
圧力法則は、他の熱力学的関係と統合され、包括的なシステム解析を可能にする。
理想気体の法則との組み合わせ:
PV = nRT 併せて P ∝ T ガスの挙動を完全に記述
熱力学的仕事の計算:
仕事=∫P dV (ボリューム変更用)
仕事=nR ∫T dV/V (圧力の法則を取り入れる)
熱伝導の関係:
Q = nCᵥΔT (定容加熱)
ΔP = (nR/V) × ΔT (加熱による圧力上昇)
圧力法則は産業用熱システムにどのように適用されるか?
圧力法則は、圧力容器から熱処理装置に至るまで、閉じ込められたガスシステム内の温度変化を伴う重要な産業用途を支配している。
圧力法則の産業応用には、圧力容器設計、熱安全システム、プロセス加熱計算、空気圧システムの温度補償などがあり、P₁/T₂=P₂/T₂は熱変化に対する圧力応答を決定する。
圧力容器設計アプリケーション
圧力法則は圧力容器設計の基本であり、さまざまな温度条件下での安全な運転を保証する。
設計圧力の計算:
設計圧力 = 最高使用圧力 × (T_max/T_operating)
熱応力解析:
硬い容器の中でガスを加熱する場合:
- 圧力上昇:p₂ = p₁ × (t₂/t₁)
- 壁応力:σ=P×r/t(薄肉近似)
- 安全マージン:熱膨張効果を考慮
デザイン例:
貯蔵容器:100 PSI、20℃で1000 L
最高使用温度:80
温度比:(80+273.15)/(20+273.15) = 353.15/293.15 = 1.205
設計圧力:100×1.205×1.5(安全係数)=180.7 PSI
熱処理システム
工業用熱処理システムは、加熱・冷却サイクル中の圧力変化を制御・予測するために圧力法則に依存している。
プロセスアプリケーション:
| プロセスタイプ | 温度範囲 | 圧力法則の応用 |
|---|---|---|
| 熱処理 | 200-1000°C | 炉内雰囲気圧力制御 |
| 化学反応器 | 100-500°C | 反応圧管理 |
| 乾燥システム | 50-200°C | 蒸気圧計算 |
| 滅菌 | 120-150°C | 蒸気圧の関係 |
プロセス制御の計算:
圧力設定値 = ベース圧力 × (プロセス温度/ベース温度)
空気圧システムの温度補償
空気圧システムは、さまざまな環境条件下で安定した性能を維持するために温度補正が必要です。
温度補償の計算式:
P_compensated = P_standard × (T_actual/T_standard)
補償申請:
- アクチュエータ力:安定した出力を維持
- フロー制御:密度の変化を補正する
- 圧力調整:温度設定値の調整
- システム・キャリブレーション:熱効果を考慮する
報酬の例
標準条件20°C (293.15 K)で100 PSI
動作温度50°C (323.15 k)
補償圧力:100 × (323.15/293.15) = 110.2 PSI
安全システム設計
圧力法則は、熱過圧状態から保護する安全システムを設計する上で極めて重要である。
安全リリーフバルブのサイジング:
リリーフ圧力 = 使用圧力 × (T_max/T_operating) × 安全係数
安全システムのコンポーネント:
- 圧力リリーフバルブ:加熱による過圧を防ぐ
- 温度モニタリング:路面温度
- 圧力スイッチ:圧力過大時のアラーム
- 断熱:被ばく温度のコントロール
熱交換器の用途
熱交換器は、圧力法則を利用して、気体が加熱または冷却される際の圧力変化を予測し、制御する。
熱交換器の圧力計算:
ΔP_thermal = P_inlet × (T_outlet - T_inlet)/T_inlet
設計上の配慮:
- 圧力降下:摩擦効果と熱効果の両方を考慮
- エキスパンション・ジョイント:熱膨張に対応
- 定格圧力:最大熱圧設計
- 制御システム:最適な圧力状態を維持
私は最近、Klaus Weberというドイツのプロセスエンジニアと仕事をした。彼の熱処理システムには圧力制御の問題があった。圧力法則を適切に適用し、温度補償圧力制御を導入することで、プロセスの安定性を73%改善し、熱関連の機器の故障を85%削減しました。
圧力法の安全性への影響は?
圧力法則は、温度上昇によって危険な圧力状態が発生する可能性があり、それを予測し、制御しなければならない産業システムにおいて、重要な安全性を意味する。
圧力法則の安全性には、熱過圧保護、圧力逃しシステム設計、温度監視要件、熱事故に対する緊急手順などが含まれ、制御不能な加熱はP₂=P₁×(T₂/T₁)に従って破局的な圧力上昇を引き起こす可能性がある。
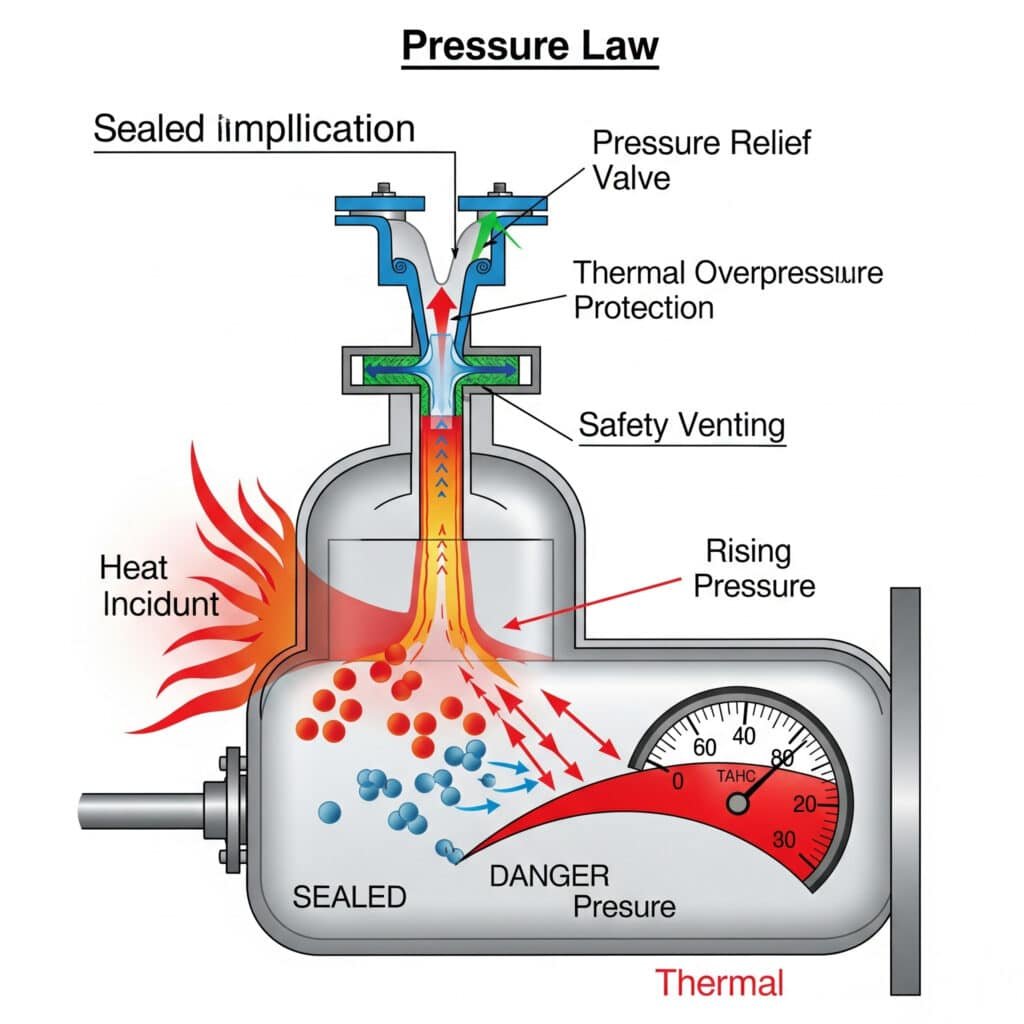
熱過圧の危険性
管理されていない温度上昇は、機器の設計限界を超える危険な圧力状態を作り出し、安全上の危険を生じさせる可能性がある。
過圧力のシナリオ:
| シナリオ | 温度上昇 | 圧力上昇 | ハザードレベル |
|---|---|---|---|
| 火への露出 | +500°C (293K~793K) | +171% | 壊滅的 |
| プロセスの動揺 | +100°C (293K~393K) | +34% | 厳しい |
| ソーラー暖房 | +50°C (293K~343K) | +17% | 中程度 |
| 機器の故障 | +200°C (293K~493K) | +68% | クリティカル |
故障モード:
- 血管破裂:過圧による致命的な故障
- シール不良:圧力/温度によるガスケットとシールの損傷
- 配管の故障:熱応力によるラインの破断
- コンポーネントの損傷:熱サイクルによる機器の故障
圧力開放システムの設計
圧力開放システムは、過圧状態に対する適切な保護を提供するために、熱圧力の上昇を考慮しなければならない。
リリーフバルブのサイジング:
リリーフ容量=最大熱圧力×流量係数
サーマルリリーフの計算:
P_relief=P_operating×(T_max/T_operating)×1.1。 (10%マージン)
リリーフシステムのコンポーネント:
- プライマリー・リリーフ:メイン圧力リリーフバルブ
- セカンダリー・リリーフ:バックアップ保護システム
- ラプチャーディスク:究極の過圧保護
- サーマル・リリーフ:特定の熱膨張保護
温度監視と制御
効果的な温度監視は、危険な状態になる前に熱状態を検知することで、危険な圧力上昇を防ぎます。
モニタリングの要件:
- 温度センサー:連続温度測定
- 圧力センサー:モニターの圧力上昇
- 警報システム:オペレーターに危険な状況を知らせる
- 自動シャットダウン:緊急システム隔離
コントロール戦略:
| 制御方法 | 応答時間 | 効果 | アプリケーション |
|---|---|---|---|
| 温度アラーム | 秒 | 高い | 早期警告 |
| 圧力インターロック | ミリ秒 | 非常に高い | 緊急シャットダウン |
| 冷却システム | 議事録 | 中程度 | 温度制御 |
| アイソレーションバルブ | 秒 | 高い | システムの分離 |
緊急時対応手順
緊急手順は、安全な対応とシステム停止を確実にするために、熱事故時の圧力法則の影響を考慮しなければならない。
緊急時のシナリオ
- 火への露出:急激な温度と圧力の上昇
- 冷却システムの故障:徐々に温度上昇
- 暴走反応:急激な温度上昇と圧力上昇
- 外部暖房:太陽熱または放射熱にさらされる
対応手順:
- 即時隔離:熱入力源の停止
- 圧力リリーフ:リリーフシステムを作動させる
- 冷却開始:緊急冷却を行う
- システムの減圧:安全に圧力を下げる
- エリア避難:人員の保護
規制遵守
安全規制では、システムの設計と運転において熱圧力の影響を考慮することが義務付けられています。
規制要件:
- ASMEボイラーコード5:圧力容器の熱設計
- API規格:プロセス機器の熱保護
- OSHA規制:熱システムにおける労働者の安全
- 環境規制:安全な熱放電
コンプライアンス戦略:
- 設計基準:公認の熱設計基準に従ってください。
- 安全性分析:サーマルハザード分析の実施
- ドキュメンテーション:熱安全記録の維持
- トレーニング:熱による危険について従業員を教育する
リスク評価と管理
包括的なリスクアセスメントには、潜在的な危険性を特定し緩和するために、熱圧力の影響を含める必要がある。
リスク評価プロセス:
- ハザードの特定:熱圧源の特定
- 結果分析:潜在的な結果を評価する
- 確率評価:発生の可能性を判断する
- リスクランキング:リスク軽減のための優先順位付け
- 緩和戦略:保護措置の実施
リスク軽減策:
- デザイン・マージン:熱効果のための特大装置
- 冗長保護:複数の安全システム
- 予防メンテナンス:システムの定期点検
- オペレーター・トレーニング:熱安全意識
- 緊急時計画:サーマルインシデント対応手順
圧力法則は他の気体法則とどのように統合されるのか?
圧力則は他の基本的な気体の法則と統合され、気体の挙動に関する包括的な理解を形成し、高度な熱力学的解析の基礎となる。
圧力則は、ボイルの法則(P₁V₁=P₂V₂)、シャルルの法則(V₁/T₁=V₂/T₂)、アボガドロの法則と統合し、複合気体の法則と理想気体の方程式PV=nRTを形成し、完全な気体挙動の記述を提供する。
ガス法統合
圧力の法則は他の気体の法則と組み合わされ、複数の性質が同時に変化する場合の気体の挙動を記述する包括的な複合気体の法則となる。
複合ガス法:
(p₁v₁)/t₁ = (p₂v₂)/t₂
この式には、この方程式が組み込まれている:
- 圧力法則:P₁/T₁=P₂/T₂ (体積一定)
- ボイルの法則:P₁V₁=P₂V₂(温度一定)
- シャルルの法則:V₁/T₁=V₂/T₂(圧力一定)
個別法の派生:
複合気体の法則より:
- V₁=V₂→P₁/T₁=P₂/T₂とする(圧力の法則)
- T₁=T₂→P₁V₁=P₂V₂とする(ボイルの法則)
- P₁=P₂→V₁/T₁=V₂/T₂とする(シャルルの法則)
理想気体の法則の発展
圧力則は、気体の挙動を最も包括的に記述する理想気体の法則に寄与している。
理想気体の法則:
PV = nRT
気体の法則からの導出:
- ボイルの法則:P ∝ 1/V (定数T, n)
- シャルルの法則:V∝T (定数P, n)
- 圧力法則:P∝T (定数V, n)
- アボガドロの法則:V ∝ n (定数P, T)
合体した: PV ∝ nT → PV = nRT
熱力学的プロセス統合
圧力法則は熱力学的プロセスと統合され、様々な条件下での気体の挙動を記述する。
プロセスの種類:
| プロセス | 定数プロパティ | 圧力法則の応用 |
|---|---|---|
| アイソコリック | ボリューム | 直接適用:P ∝ T |
| アイソバリック | 圧力 | シャルルの法則との組み合わせ |
| 等温 | 温度 | 直接の適用はない |
| 断熱 | 熱伝導なし | 修正された関係 |
アイソコリック・プロセス(一定体積):
P₁/T₁ = P₂/T₂ (直接圧力の法則の適用)
仕事=0 (音量変化なし)
Q = nCᵥΔT (熱は内部エネルギーの変化に等しい)
実ガスの挙動統合
圧力法則は、分子の相互作用と有限の分子サイズを考慮した状態方程式を通して、実際の気体の挙動に拡張される。
ファンデルワールス方程式:
(P + a/V²)(V - b) = RT
どこでだ:
- a = 分子間引力補正
- b = 分子体積補正
実ガス圧の法則:
P_real = RT/(V-b) - a/V².
圧力の法則はそのまま適用されるが、実際の気体の挙動に合わせて補正が加えられる。
運動理論の統合
圧力法則は運動論的分子理論と統合され、巨視的な気体の挙動を微視的に理解することができる。
運動理論の関係:
P = (1/3)nmv ̄²(P = (1/3)nmv ̄²)。 (微視的圧力)
v̄²∝T (速度-温度関係)
したがってP∝T (運動論による圧力の法則)
統合のメリット:
- ミクロの理解:巨視的法則の分子基盤
- 予測能力:第一原理からの行動予測
- 制限の識別:法律が崩壊する状況
- 高度なアプリケーション:複雑系解析
私は最近、韓国のパク・ミンジュンというエンジニアと仕事をしました。彼の多段圧縮システムには、統合気体法則解析が必要でした。圧力法則を他の気体法則と組み合わせて適切に適用することで、システム設計を最適化し、性能を67%向上させながら43%のエネルギー削減を達成しました。
実践的な統合アプリケーション
統合ガス法アプリケーションは、複数の変化する変数や条件を含む複雑な産業問題を解決します。
多変数問題:
- P、V、Tの同時変化:複合気体の法則を使う
- プロセスの最適化:適切な法律の組み合わせを適用する
- 安全性分析:可能なすべての変数の変更を考慮する
- システム設計:複数の気体の法則の効果を統合する
エンジニアリングの応用:
- コンプレッサー設計:圧力と体積効果の統合
- 熱交換器の分析:熱効果と圧力効果を組み合わせる
- プロセス制御:コントロールのために統合された関係を使う
- 安全システム:すべての気体の法則の相互作用を考慮する
結論
圧力の法則(ゲイ・リュサックの法則)は、気体の圧力が体積一定で絶対温度に正比例する(P₁/T₁=P₂/T₂)ことを定めており、温度変化が圧力条件に影響する熱システム設計、安全解析、工業プロセス制御に不可欠な理解を提供している。
物理学における圧力の法則に関するFAQ
物理学における圧力の法則とは?
圧力の法則はゲイ=リュサックの法則とも呼ばれ、体積と量が一定であるとき、気体の圧力は絶対温度に正比例するというもので、P₁/T₁=P/T₂またはP∝Tと表される。
圧力の法則と分子の挙動はどのように関係しているのか?
圧力法則は分子運動理論を反映したもので、温度が高いほど分子の速度が上がり、容器の壁との衝突が激しくなるため、より頻繁で強力な分子衝突によって高い圧力が発生する。
圧力法則の数学的応用とは?
数学的応用には、温度による圧力変化の計算(P₂=P₁×T₂/T₁)、圧力係数の決定(β=1/T)、適切な圧力余裕を持つ熱安全システムの設計などがある。
圧力法は労働安全にどのように適用されるのか?
産業安全アプリケーションには、圧力逃し弁のサイジング、熱過圧保護、温度監視システム、危険な圧力上昇を引き起こす可能性のある熱事故に対する緊急手順などが含まれます。
圧力の法則と他の気体の法則の違いは何ですか?
圧力の法則は体積一定で圧力と温度に関係し、ボイルの法則は温度一定で圧力と体積に関係し、シャルルの法則は圧力一定で体積と温度に関係する。
圧力の法則と理想気体の法則はどのように統合されるのですか?
圧力法則は他の気体法則と組み合わさって理想気体方程式PV = nRTを形成し、圧力-温度関係(P ∝ T)は包括的な気体挙動記述の構成要素のひとつとなる。
-
物理学における基本的な気体の法則であり、体積が一定の気体の圧力と絶対温度の直接的な関係を記述するゲイ=リュサックの法則を詳しく解説。 ↩
-
気体の法則の計算に不可欠な、粒子の振動運動が最小となる理論上の点である絶対零度を起点とする、ケルビンなどの絶対温度スケールの概念を解説。 ↩
-
気体を構成する分子の運動と相互作用を考慮することによって、気体の巨視的な性質(圧力や温度など)を説明する科学モデルである気体の運動論について概説。 ↩
-
ある温度における気体中の粒子の速度分布を規定する統計力学の確率分布であり、気体の運動論の重要な部分を形成するマックスウェル・ボルツマン分布について記述している。 ↩
-
ASMEボイラー・圧力容器コード(BPVC)は、ボイラー・圧力容器の設計・建設・検査を規制する主要規格で、熱圧効果への配慮を含む安全性を確保するための情報を提供します。 ↩


