
Плаин је агрегатно стање материје у којем се молекули слободно крећу, шире се да попуне расположиви простор и снажно реагују на промене притиска, запремине и температуре. Овај основни појам је важан у индустријским применама јер се са плинама не поступа као са течностима или чврстим материјама. У системима компримованог ваздуха, пнеуматским актуаторима, процесним посудама, цилиндрима за складиштење гаса и опреми за сагоревање, мала промена температуре или запремине може променити притисак, проток, густину и безбедносне захтеве. Разумевање понашања гаса помаже инжењерима да исправно одреде величину компоненти, избегну нестабилан рад и препознају када једноставне претпоставке идеалног гаса више нису довољне.
За индустријске читаоце, најпрактичнија тачка је једноставна: гас је користан јер се може компримовати, ширити и лако преносити кроз цеви и вентиле, али исте те особине чине да буде осетљив на губитак притиска, топлоту, цурење, контаминацију и небезбедне услове складиштења. Поуздан гасни систем не пројектује се само на основу притиска. Он такође узима у обзир температуру, запремину, састав гаса, влагу, захтев за протоком, капацитет регулатора и радно окружење.
Списак садржаја
- Шта дефинише гас као агрегатно стање материје?
- Зашто је понашање гаса важно у индустријским применама?
- Која својства гаса инжењери треба прво да разумеју?
- Како гасни закони помажу у предвиђању понашања индустријских гасова?
- Које се врсте гасова обично користе у индустрији?
- Које уобичајене грешке изазивају проблеме у гасном систему?
- Практична листа за проверу гасних и пнеуматских система
- Често постављана питања о основним концептима гаса
- Референце
Шта дефинише гас као агрегатно стање материје?
Плаин нема утврђен облик нити утврђен волумен. Он се шири док не испуни посуду или мрежу цеви која му је на располагању. У поређењу са чврстим и течним супстанцама, молекули гаса су много удаљенији, па притисак може значајно смањити волумен. Зато компримовани ваздух може складиштити енергију, зашто пнеуматски цилиндри могу померати делове машина и зашто се гасни боца морају третирати као опрема која задржава притисак, а не као обични контејнери за складиштење.
На микроскопском нивоу, притисак гаса потиче од молекуларног кретања. Притисак гаса се детектује када молекули гаса ударају у зидове посуде и стварају силу по јединици површине.[1]. Ово објашњење није само теорија у учионици. То је разлог зашто су маномети, регулатори, преливни вентили и арматура отпорна на притисак неопходни у стварној опреми.
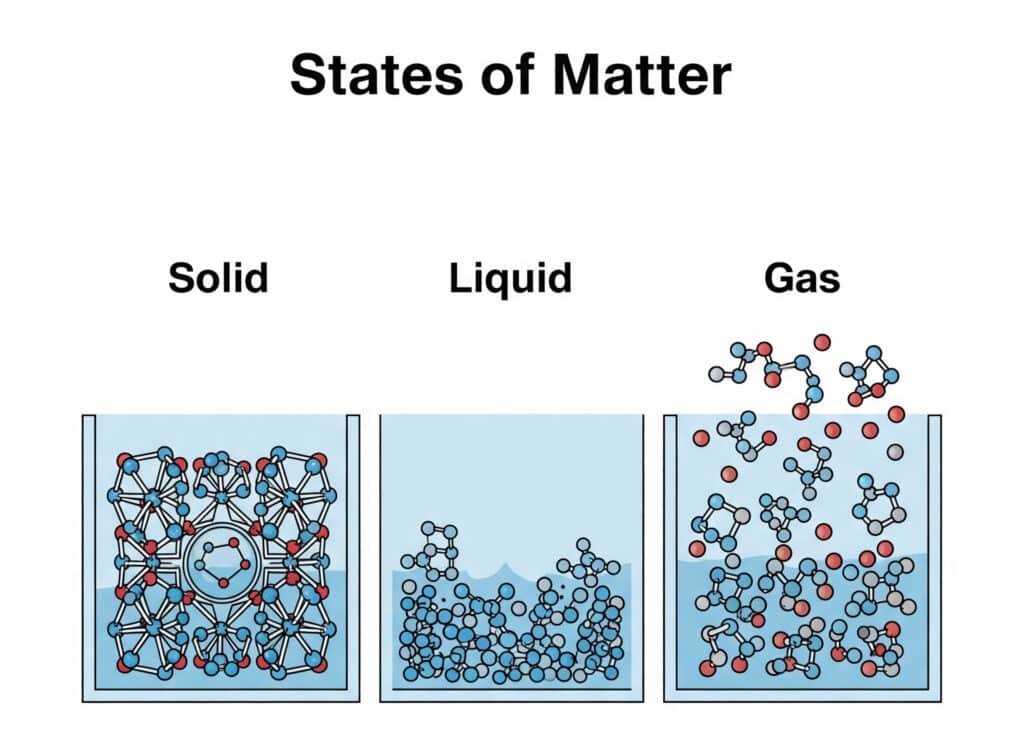
| Агрегатно стање | Облик | Обим | Индустријско значење |
|---|---|---|---|
| Чврст | Поправљено | Скоро поправљено | Користи се за рамове, кућишта, алате и конструктивне делове где је стабилност димензија важна. |
| Течност | Преузима облик контејнера | Скоро поправљено | Користи се у хидравлици, хлађењу, подмазивању и преносу хемикалија где је важна ниска компресибилност. |
| Плин | Преузима облик контејнера | Лако се шири или стиска | Користи се у пнеуматском покретању, испирању, заведовању, сагоревању, хлађењу, сушењу и притиснутом складиштењу. |
Зашто је понашање гаса важно у индустријским применама?
Понашање индустријских гасова је важно јер гасни системи ретко раде у једном фиксном режиму. Компресори загревају ваздух, дугачке цевоводне трасе изазивају пад притиска, вентили ограничавају проток, боце се убрзавају и успоравају, а резервоари за складиштење могу бити изложени променљивим спољашњим температурама. Систем који функционише у једноставној прорачунској анализи може постати нестабилан ако се занемаре стварни притисак, температура, влажност или захтев за протоком.
У пнеуматској аутоматизацији понашање гаса директно утиче на силу извршног органа, брзину, амортизацију, поновљивост и потрошњу енергије. Пнеуматски цилиндар може бити оцењен за одређени притисак, али стварни покрет зависи од расположивог протока на прикључку, одзива регулатора, пречника цеви, ограничења на испусту, трења заптивке и профила оптерећења. Зато се две машине које користе исти номинални притисак могу веома различити у понашању.
У процесима и примени у складиштењу понашање гаса утиче на безбедност. Грејање гасног контејнера фиксног обима може повећати притисак. Брзо ширење може охладити гас и створити ризик од кондензације или замрзавања. Гас обогаћен кисеоником може појачати сагоревање, док инертни гасови могу истиснути ваздух за дисање у затвореним просторима. Правилно питање у пројектовању није само “Који притисак нам је потребан?”, већ и “Шта се дешава ако се промене температура, проток, састав или садржај?”
Која својства гаса инжењери треба прво да разумеју?
Најважнија својства гаса за индустријску примену су притисак, запремина, температура, количина гаса, густина, проток, садржај влаге и хемијско понашање. Ова својства су међусобно повезана, па промена једног често утиче на више других.
| Некретнина | Шта то значи | Зашто је то важно у индустрији |
|---|---|---|
| Притисак | Сила по јединици површине коју стварају молекули гаса и задржавање. | Одређује силу актуатора, напрезање посуде, избор регулатора и заштиту од преоптерећења. |
| Обим | Простор доступан за гас. | Утиче на капацитет складиштења, величину цилиндра, потражњу за компресором и понашање експанзије. |
| Температура | Мерење повезано са молекуларном кинетичком енергијом. | Промене притиска, густине, вискозитета, ризика кондензације и граница материјала. |
| Густина | Маса гаса по јединици запремине. | Утичу на прорачун протока, понашање при подизању или седењу, вентилацију и мерење масеног протока. |
| Проток | Количина гаса која се креће по јединици времена. | Контролише брзину актуатора, ефикасност испирања, перформансе горионика и капацитет снабдевања процеса. |
| Удељ влаге | Водена пара ношена у гасу. | Може изазвати корозију, замрзавање, заглављивање вентила, лоше подмазивање и проблеме са сензорима. |
| Хемијско понашање | Да ли је гас инертан, оксидишућ, запаљив, токсичан, корозиван или реактиван. | Одређује компатибилност материјала, вентилацију, детекцију, означавање и поступке рада. |
Притисак: више од очитавања мерача
Притисак треба јасно навести као мерни притисак или апсолутни притисак. Мерни притисак упоређује притисак система са атмосферским притиском, док апсолутни притисак почиње од вакуума. Многе формуле за гасове захтевају апсолутни притисак. Мешање мерног и апсолутног притиска чест је извор погрешног одређивања величине и обмањујућих прорачуна.
Температура: скривена променљива
Температура утиче на притисак, густину и понашање влаге. У цевоводу компримованог ваздуха врући ваздух из компресора може да задржи више водене паре. Када се ваздух охлади низ ток, вода се може кондензовати и доћи до вентила или актуатора. У запечаћеном складиштењу гаса загревање може повећати притисак чак и када се не додаје додатни гас.
Густина и проток: зашто “исти притисак” не значи увек “исти учинак”
Густина гаса се мења са притиском и температуром. То утиче на то колико масе заправо пролази кроз вентил или отвор. У пнеуматским системима манометар може показивати довољан притисак у мировању, али актуатор и даље може споро да се креће ако доводна цев, вентил, прикључак или пригушивач не могу да обезбеде довољан проток при динамичком захтеву.
Како гасни закони помажу у предвиђању понашања индустријских гасова?
Закони гасова пружају практичан оквир за предвиђање како гасови реагују када се мења притисак, запремина, температура или количина гаса. То су поједностављени модели, али су корисни за првобитно одређивање димензија, отклањање кварова и разумевање узрока и последица.
Закон идеалног гаса је најчешћа полазна основа. Јаднаост стања идеалног гаса повезује притисак, температуру, густину и гасну константу.[2]. У моларном облику се пише PV = nRT, где је P апсолутни притисак, V запремина, n количина гаса, R моларна гасна константа, а T апсолутна температура.
При коришћењу СИ јединица, Моларна гасна константа је наведена од стране NIST-а као 8,314 462 618… Џ мол⁻¹ К⁻¹[3]. У практичном инжењерском раду исправан систем јединица је подједнако важан као и формула. Исправна једначина са мешовитим јединицама и даље може дати небезбедан одговор.
| Планински закон или процес | Једноставна веза | Користан индустријски пример | Практична опрезност |
|---|---|---|---|
| Бојлов закон | При константној температури притисак и запремина се крећу у супротним правцима. | Процена како компресија мења притисак или капацитет складиштења. | Правилна компресија често загрева гас, па температура можда неће остати константна. |
| Чарлсов закон | При константном притиску, запремина се повећава са порастом апсолутне температуре. | Процена проширења у процесима грејања, сушења и вентилације. | Користите апсолутну температуру, а не Целзијус или Фаренхајт директно. |
| Геј-Лусаков закон | При константном волумену, притисак расте како апсолутна температура расте. | Процена пораста притиска у затвореним посудама изложеним топлоти. | Никада не претпостављајте да је затворени гасни контејнер безбедан само зато што је почетни притисак низак. |
| Закон о мешању гасова | Притисак, запремина и температура могу бити повезани за фиксну количину гаса. | Упоређивање стања складиштења или процеса пре и после промена температуре и притиска. | Масовни цурење, кондензација и промене фазе могу поништити једноставан модел. |
| Понашање правог гаса | За стварне гасове могу бити потребни корекциони фактори при високом притиску, ниској температури или у близини фазне промене. | Складиштење под високим притиском, специјални гасови, хладива и процесни гасови. | Користите податке добављача или одговарајућу једначину стања за критичне примене. |
Где претпоставке идеалног гаса добро функционишу
Рачунања идеалног гаса често су довољна за обичан ваздух, азот, кисеоник и сличне гасове при умереним притисцима и температурама, када је гас далеко од стања кондензације или критичних услова. Корисна су за процену промена запремине, промена притиска, трендова густине и општег пнеуматског понашања.
Где претпоставке идеалног гаса постају ризичне
Претпоставке идеалног гаса постају мање поуздане при високом притиску, ниској температури, близу течења или код гасова са јаким молекуларним интеракцијама. У тим случајевима инжењери треба да користе податке о стварним гасовима, факторе компресибилности, техничке податке добављача или алате за симулацију процеса. Ово је посебно важно за складиштење под високим притиском, хладњаче, криогене гасне системе и специјалне процесне гасове.
Које се врсте гасова обично користе у индустрији?
Индустријски гасови се бирају по функцији, а не само по доступности. Гас може бити изабран зато што је инертан, реактиван, оксидишући, запаљив, сув, чист, јефтин, лако комприметан или компатибилан са процесним материјалом. Исти гас може бити безбедан у једном окружењу, а опасан у другом.
| Категорија горива | Уобичајени примери | Главне индустријске примене | Кључни ризик за проверу |
|---|---|---|---|
| Компримовани ваздух | Ваздух за постројење, инструментални ваздух, осушени ваздух | Пнеуматски цилиндри, вентили, алати, одводник, управљачки системи. | Влага, уље, пад притиска, контаминација, нестабилан проток. |
| Инертни гасови | Азот, аргон, хелијум | Премазивање, прочишћавање, заваривачко заклоњење, испитивање цурења. | Исмештање кисеоника и задушење у слабо проветреним просторима. |
| Оксидишући гасови | Кисеоник, кисеоником обогаћене мешавине | Сагоревање, сечење, медицинске и процесне примене. | Повећана интензивност пожара и захтеви за компатибилношћу материјала. |
| Горивни гасови | Природни гас, пропан, водоник, ацетилен | Грејање, сечење, заваривање, сагоревање, енергетски системи. | Пожар, експлозија, детекција цурења, вентилација, извори паљења. |
| Реактивни или токсични гасови | Амонијак, хлор, сумпор диоксид и други | Хемијска производња, хлађење, прерада воде, процесне реакције. | Токсична изложеност, корозија, хитна интервенција, компатибилни материјали. |
| Специјалне гасове | Калибрациони гасови, ултра-високочисти гасови, мешани гасови | Инструментација, лабораторије, полупроводнички процеси, контрола квалитета. | Чистоћа, трагова контаминације, руковање цилиндрима и документација. |
Компримовани ваздух заслужује посебну пажњу јер је толико уобичајен да га тимови понекад потцењују. Ваздух делује безопасно, али компримовани ваздух садржи складиштену енергију и може да носи воду, уљни маглац, честице и пулсације притиска. За пнеуматску опрему квалитет ваздуха и проток често су подједнако важни као и номинални притисак.
Пластика боца такође захтевају дисциплиновано руковање. OSHA захтева од послодаваца да утврде да су боце са компримованим гасом под њиховом контролом у безбедном стању, у оној мери у којој се то може утврдити визуелним прегледом.[4]. Ово потврђује практилно правило: никада не сматрајте цилиндар, регулатор, црево или вентил прихватљивим само зато што су прошлог пута успешно функционисали.
Класификација опасности такође је важна. Гасови под притиском се класификују уз упозорења као што су "садржи гас под притиском и може експлодирати при загревању"[5]. Хлађени течни гасови представљају другачији ризик јер веома ниска температура може изазвати криогене опекотине или повреде.
Које уобичајене грешке изазивају проблеме у гасном систему?
Многи кварови у гасним системима не настају због непознавања формуле. Они настају применом формуле без разумевања околних услова. Најчешће грешке су практичне, а не теоријске.
- Коришћење мерног притиска у формулама које захтевају апсолутни притисак. Ово може искривити процене густине, запремине и протока.
- Под претпоставком да је притисак једнак протоку. Систем може да показује тачан статички притисак, а ипак ускраћивао актуатору уље током кретања.
- Игнорисање пораста температуре током компресије. Компресиона топлота утиче на притисак, понашање влаге, век трајања мазива и стање заптивке.
- Прекомерно или недовољно величине регулатора и вентила. Регулатор који по величини прикључка изгледа исправно можда неће обезбедити потребни проток при захтеваном паду притиска.
- Заборављање влаге у компримованом ваздуху. Вода може кородирати делове, зачепити мале пролазе, смрзнути се у хладним подручјима и смањити пнеуматску поузданост.
- Третирање свих гасова као ваздуха. Кисеоник, водоник, амонијак, азот, аргон и CO₂ имају различите опасности и захтеве за компатибилност.
- Игнорисање ограничења издувних гасова. Пригушивачи, брзи издувни вентили и мале цевчице могу променити брзину актуатора и понашање пригушивања.
- Прескакање провера цурења. Мале цурења гаса расипају енергију, смањују стабилност притиска и у зависности од врсте гаса могу представљати ризик од пожара, тровања или гушења.
Практична листа за проверу гасних и пнеуматских система
Пре него што изаберете компоненте или отклоните квар на гасном систему, најпре прикупите основне информације о раду. Ово спречава уобичајен проблем избора делова само на основу номиналног притиска.
- Идентификујте тип гаса, чистоћу, влажност и класификацију опасности.
- Забележите притисак напајања, радни притисак, очекивано смањење притиска и да ли су вредности мерни или апсолутни.
- Дефинишите минималну и максималну радну температуру, укључујући покретање, заустављање и изложеност околини.
- Процените потражњу за протоком током реалног рада, а не само у условима стабилног режима.
- Проверите дужину цеви, унутрашњи пречник, прикључке, пригушиваче, регулаторе, вентиле и ограничења.
- Потврдите материјалску компатибилност за заптивке, мазива, метале, пластике и премазе.
- Проверите да ли се гас може кондензовати, течнити, смрзнути, реаговати или контаминирати процес.
- Потврдите да су боце, посуде, црева, регулатори и арматуре означени за стварни притисак и гасну службу.
- Планирајте вентилацију, откривање цурења, означавање, одржавање и хитни одговор где је то потребно.
- За пнеуматски покрет тестирајте брзину, силу, амортизацију, поновљивост и време опоравка под стварним оптерећењем.
Како се ово односи на пнеуматску аутоматизацију?
Пнеуматска аутоматизација користи понашање гаса на контролисан начин. Компримовани ваздух складишти енергију, вентили усмеравају ту енергију, а извршни органи је претварају у кретање. Основни концепт гаса објашњава зашто су пнеуматски системи брзи, једноставни и флексибилни, али и зашто су осетљиви на квалитет ваздуха, цурење, пад притиска и нестабилно снабдевање током.
При избору пнеуматских компоненти почните са потребном силом и брзином, а затим проверите расположиву залиху ваздуха. Већи цилиндар може да произведе већу силу, али и троши више ваздуха. Мањи вентил може да смањи трошкове, али може да ограничи брзину. Дужи цревовод може да поједностави распоред машине, али може да успори одговор. Добар дизајн балансира притисак, проток, величину цилиндра, капацитет вентила, дужину црева и захтеве за управљање.
За тимове за одржавање, најбољи редослед отклањања кварова обично је визуелна инспекција, провера притиска, детекција цурења, провера квалитета ваздуха, провера ограничења протока, а затим замена компоненти само када докази указују на неисправан део. Замена цилиндара или вентила без провере услова снабдевања гасом често само на кратко прикрива изворни проблем.
Често постављана питања о основним концептима гаса
Који је основни концепт гаса?
Плаин је агрегатно стање материје у којем се молекули слободно крећу, шире се да попуне расположиви простор и значајно мењају запремину када се промени притисак или температура. То чини плаин корисним за компресију, проток, испирање и пнеуматски покрет, али такође захтева пажљиву контролу.
Зашто су гасови лакши за компримовање од течности?
Гасове је лакше компримовати јер су њихове молекуле много удаљеније него молекуле течности. Притисак може да смањи простор између молекула гаса, док течности имају много мање слободног простора за смањење.
Зашто се притисак гаса повећава када температура порасте?
Када температура порасте, молекули гаса се крећу са више енергије. У фиксном обиму они снажније и чешће ударају у зидове посуде, па притисак расте. Ово је важно за запечаћене посуде, боце и опрему изложене топлоти.
Да ли је компримовани ваздух исто што и индустријски гас?
Компримовани ваздух је једна од врста индустријског снабдевања гасом, али се не понашају сви индустријски гасови као компримовани ваздух. Азот, кисеоник, аргон, водоник, амонијак, CO₂ и специјалне мешавине имају различите захтеве у погледу безбедности, чистоће, компатибилности материјала и руковања.
Која је најчешћа грешка у прорачунима пнеуматских гасова?
Најчешћа грешка је претпоставити да само притисак одређује перформансе. Пнеуматске перформансе такође зависе од проточног капацитета, пречника црева, Cv вредности вентила, одзива регулатора, ограничења на испусту, квалитета ваздуха и услова оптерећења.
Када треба узети у обзир понашање идеалног гаса?
Понашање стварног гаса треба узети у обзир при високом притиску, ниској температури, близу кондензације или ликвификације, или када се ради са специјалним гасовима. У тим случајевима користите податке добављача, инжењерски софтвер или одговарајуће једначине стања уместо да се ослањате само на закон идеалног гаса.
Закључак
Основни концепт гаса није само научна дефиниција. То је практичан инжењерски алат. Гасови испуњавају расположиви простор, компримују се под притиском, шире се са температуром, пролазе кроз сужења и стварају притисак кроз молекуларно кретање. У индустријским применама ова понашања утичу на брзину извршног органа, оптерећење компресора, безбедност складиштења, чистоћу гаса, компатибилност материјала и стабилност процеса. Најбезбеднији и најпоузданији системи дизајнирају се узимајући у обзир притисак, запремину, температуру, проток, врсту гаса и радно окружење заједно.
Ако бирате пнеуматске цилиндре, вентиле, јединице за припрему ваздуха или прикључке за аутоматизациони пројекат, припремите радни притисак, потребну силу, ход, брзину циклуса, квалитет ваздуха и радно окружење пре упоређивања опција. Ове информације помажу добављачима и инжењерима да препоруче компоненте које одговарају стварном понашању гаса, а не само каталошком притиску.
Референце
- Истраживачки центар Глен НАСА — Пritisак гаса. Приступљено 2026-05-21. Улога доказа: механизам; Тип извора: влада. Подржава: Објашњење да притисак гаса настаје услед судара молекула гаса са зидовима посуде и деловања силе по јединици површине. ↩
- НАСА Глен истраживачки центар — Једначина стања / Идеални гас. Приступљено 2026-05-21. Улога доказа: општа_подршка; Тип извора: владина. Подршка: Коришћење једначине стања идеалног гаса за повезивање притиска, температуре, густине и гасне константе. ↩
- NIST CODATA вредност: моларна гасна константа. Приступљено 2026-05-21. Улога доказа: статистички; Тип извора: владина. Подршка: наведена SI вредност моларне гасне константе коришћене у идеалним гасним прорачунима. ↩
- OSHA 29 CFR 1910.101 — Компримовани гасови, општи захтеви. Приступљено 2026-05-21. Улога доказа: general_support; Тип извора: government. Подршка: Захтев да послодавци утврде да ли су боце са компримованим гасом под њиховом контролом у безбедном стању, колико то визуелним прегледом може да се утврди. Напомена о обиму: Овај извор одражава захтеве америчке OSHA и треба га проверити у односу на локалне прописе за радња места ван САД. ↩
- Канадски центар за здравље и безбедност на раду — Опасни производи користећи пиктограм гасног боца. Приступљено 2026-05-21. Улога доказа: general_support; Тип извора: government. Подршка: Тачка за комуникацију о опасностима да притиснути гасови могу садржати упозорења као што су "садржи притиснути гас и може експлодирати при загревању", са посебним упозорењима за расхлађене течне гасове. ↩


