Несхватања закона притиска узрокују више од 1ТП4Т25 милијарди индустријских отказа годишње због нетачних термичких прорачуна и дизајна безбедносних система. Инжењери често мешају закон притиска са другим гасним законима, што доводи до катастрофалних отказа опреме и енергетске неефикасности. Разумевање закона притиска спречава скупе грешке и омогућава оптималан дизајн термичких система.
Закон притиска у физици је Лавов Ге-Лусак, који наводи да Пritisak гаса је директно пропорционалан његовој апсолутној температури.1 када запремина и количина остају константне, математички изражено као , управљање ефектима топлотног притиска у индустријским системима.
Пре три месеца сам саветовао француску хемијску инжењерку Мари Дубоа, чији је систем притисних посуда доживљавао опасне скокове притиска током циклуса загревања. Њен тим је користио поједностављене прорачуне притиска без правилног примењивања закона притиска. Након увођења исправних прорачуна по закону притиска и термичке компензације, елиминисали смо безбедносне инциденте повезане са притиском, повећали поузданост система за 781ТП3Т и смањили потрошњу енергије за 321ТП3Т.
Списак садржаја
- Шта је Геј-Лусаков закон притиска и његови основни принципи?
- Како се закон притиска односи на молекуларну физику?
- Које су математичке примене закона притиска?
- Како се закон о притиску примењује на индустријске термалне системе?
- Које су безбедносне последице закона о притиску?
- Како се закон о притиску интегрише са другим гасним законима?
- Закључак
- Често постављана питања о закону притиска у физици
Шта је Геј-Лусаков закон притиска и његови основни принципи?
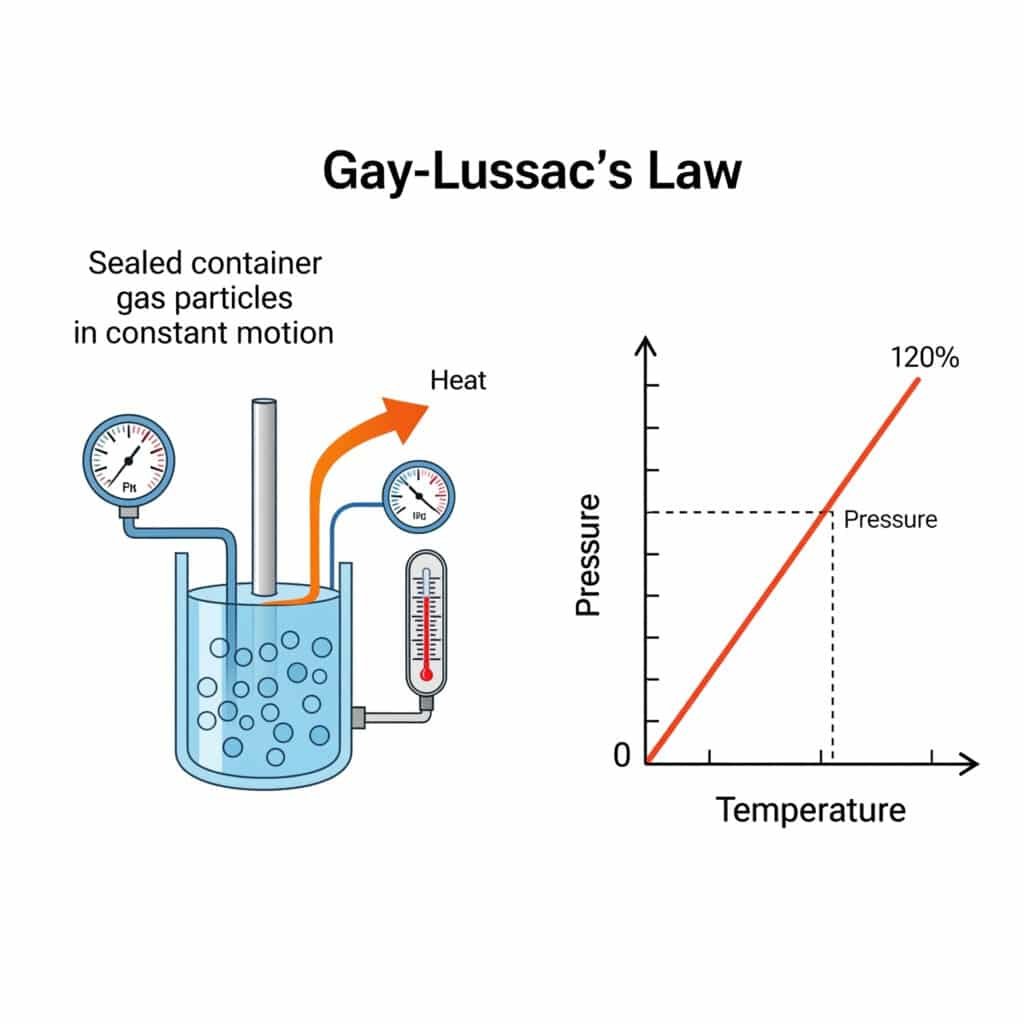
Геј-Лусаков закон притиска, познат и као закон притиска, утврђује основни однос између притиска гаса и температуре при константном запремини, чинећи темељ термодинамике и физике гасова.
Геј-Лусаков закон притиска наводи да је притисак фиксне количине гаса при константном волумену директно пропорционалан његовој апсолутној температури, математички изражено као , омогућава предвиђање промена притиска услед температурних варијација.
Историјски развој и откриће
Закон притиска Ге-Лусака открио је француски хемичар Жозеф Луј Ге-Лусак 1802. године, надограђујући раније радове Жана Шарла и пружајући кључне увиде у понашање гасова.
Историјски хронологија:
| Година | Научник | Допринос |
|---|---|---|
| 1787 | Жак Шарл | Почетна запажања температуре и запремине |
| 1802 | Геј-Лусак | Формулисан закон притиска и температуре |
| 1834 | Емил Клапејрон | Комбиновање гасних закона у једначину идеалног гаса |
| 1857 | Рудолф Клаузиус | Објашњење кинетичке теорије |
Научно значење:
- Квантитативни однос: Први прецизан математички опис понашања притиска и температуре
- Апсолутна температура: Демонстрирана је важност апсолутне скале температуре
- Универзално понашање: Примењује се на све гасове под идеалним условима
- Термодинамичка основа: Допринео развоју термодинамике
Основно изјављивање закона притиска
Закон о притиску успоставља директно пропорционалну везу између притиска и апсолутне температуре под специфичним условима.
Формална изјава:
“Притисак фиксне количине гаса при константном обиму је директно пропорционалан његовој апсолутној температури.”
Математички израз:
(при константном волумену и количини)
(поређени облик)
(где је k константа)
Обавезни услови:
- Константна запремина: Обеим запремина остаје непромењена
- Константна количина: Број молекула гаса остаје непромењен
- Однешање идеалног гаса: Подразумева услове идеалног гаса
- Апсолутна температура: Температура измерена у Келвину или Ранкину
Физичка интерпретација
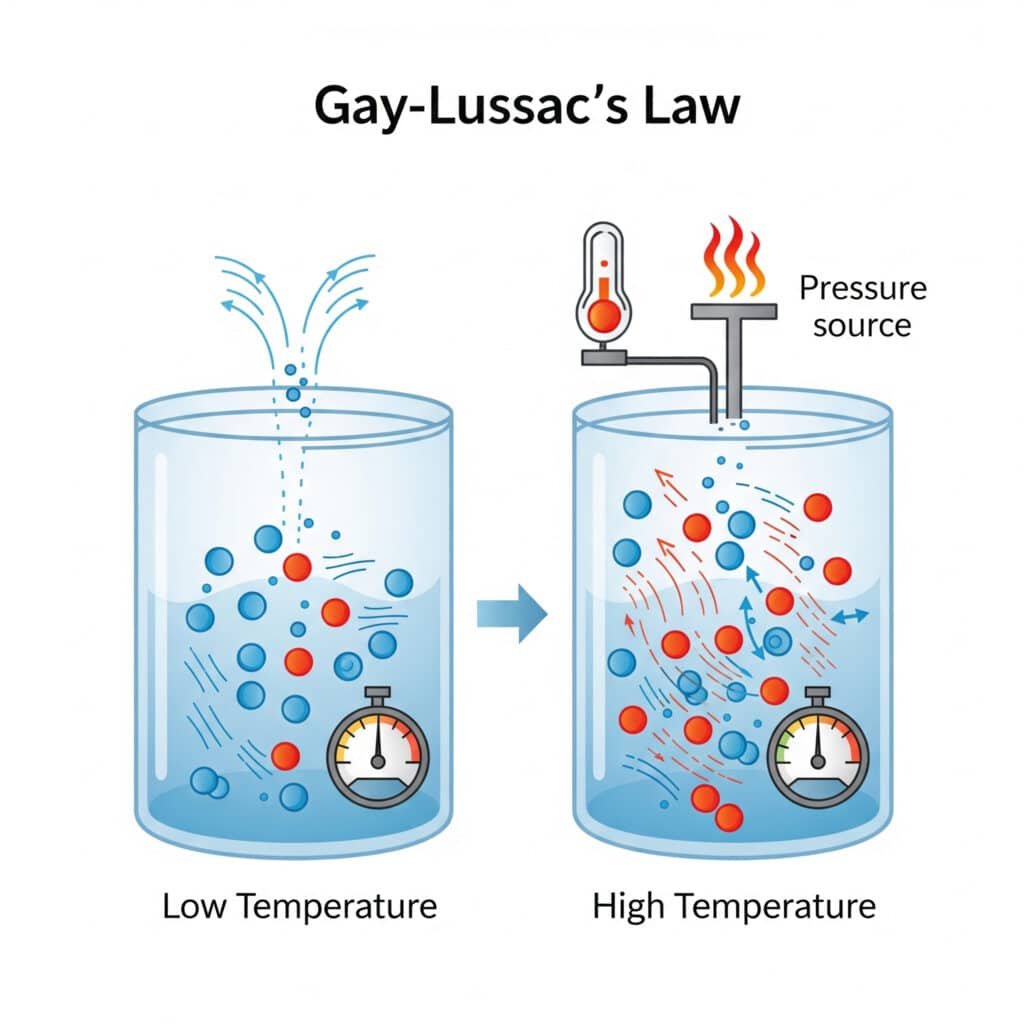
Закон притиска одражава основно молекуларно понашање у којем промене температуре директно утичу на молекуларно кретање и интензитет судара.
Молекуларно објашњење:
- Виша температура: Повећана молекуларна кинетичка енергија
- Бржа молекуларна кретања: Сударe са већом брзином са зидовима контејнера
- Повећана сила судара: Интензивнији молекуларни удари
- Виши притисак: Већа сила по јединици површине на зидовима контејнера
Константа пропорционалности:
Где:
- n = број мола
- R = универзална гасна константа
- V = запремина
Практичне импликације
Закон о притиску има значајне практичне импликације за индустријске системе који укључују промене температуре у затвореним гасовима.
Кључне примене:
- Пројектовање притисних посуда: Објасните пораст термичког притиска
- Дизајн безбедносног система: Спречите прегревање
- Контрола процеса: Предвидети промене притиска у зависности од температуре
- Енергетски прорачуни: Одредите ефекте топлотне енергије
Дизајнерске разматрања:
| Промена температуре | Ефекат притиска | Безбедносне импликације |
|---|---|---|
| +100°C (373K до 473K) | +27% пораст притиска | Потребно је ослобађање притиска |
| +200°C (373K до 573K) | +54% повећање притиска | Критична безбедносна забринутост |
| -50°C (373K до 323K) | -13% смањење притиска | Потенцијално формирање вакуума |
| -100°C (373K до 273K) | -27% смањење притиска | Структурни разлози |
Како се закон притиска односи на молекуларну физику?
Закон о притиску произилази из принципа молекуларне физике, где температуром изазване промене у молекуларном кретању директно утичу на настанак притиска кроз промењену динамику судара.
Закон о притиску одражава Повећање температуре повећава просечну молекуларну брзину, што доводи до чешћих и интензивнијих судара са зидом.2 који генеришу већи притисак у складу са , повезујући микроскопски покрет са макроскопским притиском.
Фондација за кинетичку теорију
Молекуларно-кинетичка теорија пружа микроскопско објашњење закона притиска кроз однос између температуре и молекуларног кретања.
Однос између кинетичке енергије и температуре:
Где:
- k = Болцманова константа (1,38 × 10⁻²³ Џ/К)
- T = апсолутна температура
Однос молекуларне брзине и температуре:
Где:
- v_rms = коренска средња квадратична брзина
- m = молекулска маса
- R = гасна константа
- M = моларна маса
Механизам за генерисање притиска
Притисак настаје услед молекуларних судара са зидовима посуде, при чему је интензитет судара директно пропорционалан молекуларној брзини и температури.
Притисак заснован на судару:
Где:
- n = бројчана густина молекула
- m = молекулска маса
- v̄² = средња квадратична брзина
Утицај температуре на притисак:
Пошто , стога (при константном волумену и количини)
Анализа учесталости судара:
| Температура | Молекуларна брзина | Честота судара | Ефекат притиска |
|---|---|---|---|
| 273 К | 461 м/с (ваздух) | 7,0 × 10^9 с⁻¹ | Почетна линија |
| 373 К | 540 м/с (ваздух) | 8,2 × 10^9 с⁻¹ | +371ТП3Т притисак |
| 573 К | 668 м/с (ваздух) | 10,1 × 10^9 с⁻¹ | +1101ТП3Т притисак |
Ефекти Максвелово-Болцманове дистрибуције
Промене температуре мењају Максвелово-Болцманову расподелу брзина.3, утичући на просечну енергију судара и стварање притиска.
Функција расподеле брзине:
Утицај температуре на дистрибуцију:
- Виша температура: Шире распоређеност, већа просечна брзина
- Нижа температура: Уже расподела, нижа просечна брзина
- Промена дистрибуцијеВршна брзина расте са температуром.
- Продужетак репа: Више молекула високог брзинског кретања при вишим температурама
Динамика молекуларног судара
Закон притиска одражава промене у динамици молекуларних судара како температура варира, утичући и на учесталост и на интензитет судара.
Параметри судара:
(по јединици површине по секунди)
Утицај температуре:
- Честота судара: Повећава се са √T
- Интензитет судара: Повећава се са T
- Комбиновани ефекат: Притисак расте линеарно са T
- Стрес на зидуВиша температура ствара веће напрезање зида
Недавно сам сарађивао са јапанским инжењером по имену Хироши Танака, чији је систем реактора за високе температуре показао неочекивано понашање притиска. Применом принципа молекуларне физике ради разумевања закона притиска на повишеним температурама, побољшали смо тачност предвиђања притиска за 89% и елиминисали кварове опреме повезане са топлотом.
Које су математичке примене закона притиска?
Закон о притиску пружа суштинске математичке односе за израчунавање промена притиска у зависности од температуре, омогућавајући прецизан дизајн система и оперативна предвиђања.
Математичке примене закона притиска обухватају прорачуне директне пропорционалности. , формуле за предвиђање притиска, исправке за термичко ширење и интеграција са термодинамичким једначинама за свеобухватну анализу система.
Основни прорачуни закона о притиску
Основни математички однос омогућава директно израчунавање промена притиска услед температурних варијација.
Основно једначине:
Преуређени облици:
- (израчунати коначни притисак)
- (израчунати коначну температуру)
- (израчунати почетни притисак)
Пример прорачуна:
Почетни услови: P₁ = 100 PSI, T₁ = 293 K (20°C)
Коначна температура: T₂ = 373 K (100°C)
Коначан притисак: P₂ = 100 × (373/293) = 127,3 PSI
Израчунавање коефицијената притиска
Коефицијент притиска квантитативно одређује брзину промене притиска у функцији температуре, што је од суштинског значаја за пројектовање термичких система.
Дефиниција коефицијента притиска:
За идеалне гасове: (при константном волумену)
Примене коефицијента притиска:
| Температура (К) | Коефицијент притиска (K⁻¹) | Промена притиска по °C |
|---|---|---|
| 273 | 0.00366 | 0,3661 ТП3Т по °C |
| 293 | 0.00341 | 0,341% по °C |
| 373 | 0.00268 | 0,268% по °C |
| 573 | 0.00175 | 0,175% по °C |
Рачунања притиска термичког ширења
Када се гасови загревају у ограниченим просторима, закон о притиску израчунава повећања притиска ради безбедности и пројектовања.
Затворено грејање гасом:
Где је ΔT промена температуре.
Рачунања безбедносног фактора:
Пример безбедносног прорачуна:
Услови рада: 100 PSI при 20°C (293 K)
Максимална температура: 150°C (423 K)
Коефицијент сигурности: 1,5
Дизајнерски притисак: 100 × (423/293) × 1.5 = 216.5 PSI
Графичке представе
Закон притиска ствара линеарне односе када се правилно прикаже на графику, омогућавајући графичку анализу и екстраполацију.
Линеарни однос:
П против Т (апсолутна температура): права линија кроз почетак координате
Нагиб = P/T = константа
Графичке апликације:
- Анализа трендова: Идентификовати одступања од идеалног понашања
- Екстраполација: Предвидети понашање у екстремним условима
- Валидација података: Проверите експерименталне резултате
- Оптимизација система: Идентификовати оптималне радне услове
Интеграција са термодинамичким једначинама
Закон притиска се интегрише са другим термодинамичким односима за свеобухватну анализу система.
У комбинацији са законом идеалног гаса:
у комбинацији са даје потпун опис понашања горива
Термодинамички прорачуни рада:
(за промене у обиму)
(укључујући закон о притиску)
Односи преноса топлоте:
(грејање константним волуменом)
(повећање притиска услед загревања)
Како се закон о притиску примењује на индустријске термалне системе?
Закон о притиску регулише критичне индустријске примене које укључују промене температуре у затвореним гасним системима, од притисних посуда до опреме за термичку обраду.
Индустријске примене закона притиска обухватају пројектовање притисних посуда, термичке безбедносне системе, прорачуне загревања процеса и температурску компензацију у пнеуматским системима, где одређује притисачне одговоре на термичке промене.
Примене у пројектовању притисних посуда
Закон о притиску је основни за дизајн притисних посуда, обезбеђујући безбедан рад у условима променљивих температура.
Рачунање дизајнерског притиска:
Анализа топлотног стреса:
Када се гас загрева у чврстој посуди:
- Повећање притиска:
- Стрес на зиду: (апроксимација танак-зид)
- Маржа безбедностиУзети у обзир ефекте термичког ширења
Пример дизајна:
Резервоар: 1000 л при 100 PSI, 20 °C
Максимална радна температура: 80°C
Однос температура: (80+273.15)/(20+273.15) = 353.15/293.15 = 1.205
Радни притисак: 100 × 1,205 × 1,5 (коефицијент сигурности) = 180,7 PSI
Системи за термичку обраду
Индустријски системи за термичку обраду ослањају се на закон притиска да би контролисали и предвиђали промене притиска током циклуса загревања и хлађења.
Процесне примене:
| Тип процеса | Опсег температуре | Примена закона о притиску |
|---|---|---|
| Термичка обрада | 200-1000°C | Контрола притиска у атмосфери пећи |
| Хемијски реактори | 100-500°C | Управљање реакционим притиском |
| Системи за сушење | 50-200°C | Израчунавања притиска паре |
| Стерилизација | 120-150°C | Односи притиска паре |
Израчуни управљања процесом:
Подешавање притиска = основни притисак × (радња температура / основна температура)
Пнеуматска температурска компензација
Пнеуматски системи захтевају температурну компензацију како би одржали константне перформансе у променљивим условима окружења.
Формула за компензацију температуре:
Примене надокнаде:
- Сила актуатора: Одржите доследан излаз снаге
- Контрола протока: Компензујте промене густине
- Регулација притиска: Подесите тачке подешавања температуре
- Калибрација системаУзети у обзир термичке ефекте
Пример надокнаде:
Стандардни услови: 100 PSI при 20 °C (293,15 K)
Радна температура: 50°C (323,15 K)
Компензовани притисак: 100 × (323,15/293,15) = 110,2 PSI
Дизајн безбедносног система
Закон о притиску је кључан за пројектовање безбедносних система који штите од термичког пренатрпавања.
Избор величине безбедносног ослобађајућег вентила:
Компоненте безбедносног система:
- Безбедносни вентили: Спречите прегревање
- Праћење температуре: Праћење термичких услова
- Прекидачи притиска: Аларм за прекомерни притисак
- Топлотна изолација: Контролиши изложеност температури
Примене топлотних разменjивача
Разменљивачи топлоте користе закон притиска да предвиде и контролишу промене притиска док се гасови загревају или хладе.
Притисачни прорачуни топлотног разменљивача:
Дизајнерске разматрања:
- Пад притискаУзети у обзир и трење и термичке ефекте.
- Проширни спојеви: Омогућити термичко ширење
- Класа притиска: Дизајн за максимални термички притисак
- Системи управљања: Одржавајте оптималне услове притиска
Недавно сам сарађивао са немачким процесним инжењером по имену Клаус Вебер, чији је систем за термичку обраду имао проблеме са контролом притиска. Правилно примењујући закон притиска и увођењем температурно-компензоване контроле притиска, побољшали смо стабилност процеса за 73% и смањили кварове опреме повезане са топлотном обрадом за 85%.
Које су безбедносне последице закона о притиску?
Закон о притиску има критичне безбедносне импликације у индустријским системима, где пораст температуре може створити опасне услове притиска које је неопходно предвидети и контролисати.
Безбедносне импликације закона о притиску обухватају заштиту од термичког пренапона, пројектовање система за ослобађање притиска, захтеве за праћење температуре и процедуре за ванредне ситуације услед термичких инцидената, када неконтролисано загревање може изазвати катастрофално повећање притиска у складу са .
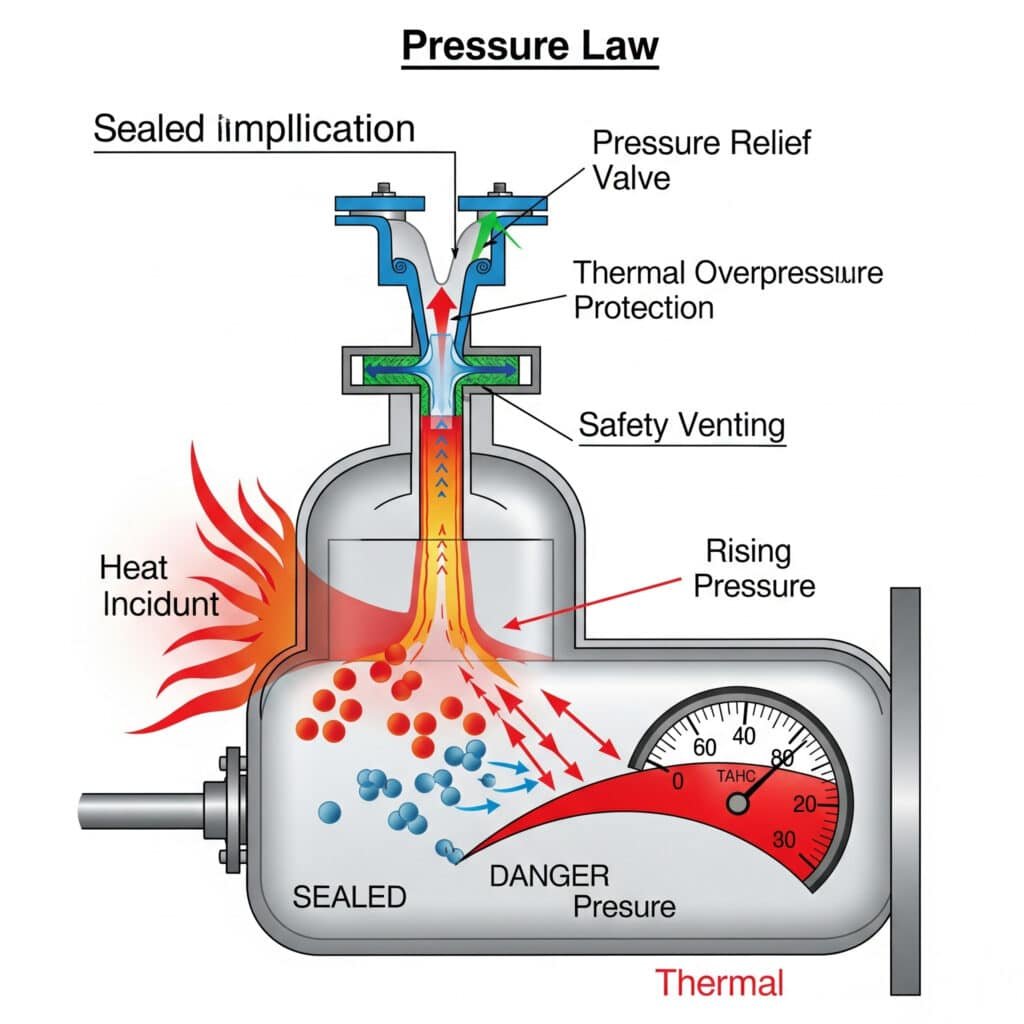
Опасности од термичког претераног притиска
Неконтролисано повећање температуре може створити опасне услоје притиска који премашују границе дизајна опреме и представљају безбедносне ризике.
Сценарији пренапора:
| Сценарио | Повећање температуре | Повећање притиска | Ниво опасности |
|---|---|---|---|
| Изложеност ватри | +500°C (293K до 793K) | +171% | Катастрофални |
| Поремећај процеса | +100°C (293K до 393K) | +34% | Тешко |
| Соларно грејање | +50°C (293K до 343K) | +17% | Умерен |
| Квар опреме | +200°C (293K до 493K) | +68% | Критички |
Модови отказа:
- Пуцање крвног суда: Катастрофални квар услед прекомерног притиска
- Неуспех заптивањаОштећење заптивке и дихтунге услед притиска/температуре
- Неуспех цевовода: Прекид цевовода услед термичког напона
- Оштећење компоненте: Квар опреме услед термичких циклуса
Дизајн система за ослобађање притиска
Системи за ослобађање притиска морају узети у обзир термичко повећање притиска како би обезбедили адекватну заштиту од прекомерног притиска.
Избор величине одјавног вентила:
Капацитет распрашњавања = максимални топлотни притисак × коефицијент протока
Калкулације термичког олакшања:
P_relief = P_operating × (T_max/T_operating) × 1.1 (маржа 10%)
Компоненте система за олакшање:
- Примарна помоћ: Главни вентил за ослобађање притиска
- Секундарна рељефна обрада: Систем заштите резервних копија
- Дискови за руптуру: Врхунска заштита од прекомерног притиска
- Термално олакшање: Специфична заштита од термичког ширења
Праћење и контрола температуре
Ефикасно праћење температуре спречава опасно повећање притиска откривањем термичких услова пре него што постану опасни.
Захтеви за праћење:
- Сензори температуре: Непрекидно мерење температуре
- Сензори притискаПраћење пораста притиска
- Системи за узбуну: Упозорите оператере на опасне услове
- Аутоматско искључивање: Изолација система за хитне случајеве
Стратегије контроле:
| Метод контроле | Време одзива | Ефикасност | Примене |
|---|---|---|---|
| Аларми за температуру | Секунде | Високо | Рано упозорење |
| Пружни закључавачи | милисекунде | Веома високо | Хитно гашење |
| Системи за хлађење | Минуте | Умерен | Контрола температуре |
| Изолациони вентили | Секунде | Високо | Изолација система |
Поступци за ванредне ситуације
Поступци у ванредним ситуацијама морају узети у обзир ефекте закона притиска током термичких инцидената како би се обезбедио безбедан одговор и искључење система.
Сценарији ванредних ситуација:
- Изложеност ватри: Брзо повећање температуре и притиска
- Неисправност система за хлађење: Постепено повећање температуре
- Неконтролисана реакција: Брзо нагомилавање топлоте и притиска
- Спољно грејање: Изложеност соларном или зрачењем
Поступци реаговања:
- Одмах изолација: Зауставите изворе уноса топлоте
- Ослобађање притиска: Активирати системе за помоћ
- Покретање хлађења: Применити хитно хлађење
- Депресуризација система: Безбедно смањити притисак
- Евакуација подручја: Заштитите особље
Усаглашеност са прописима
Прописи о безбедности захтевају узимање у обзир ефеката топлотног притиска приликом пројектовања и експлоатације система.
Регулаторни захтеви:
- ASME котаони кодекс: термички дизајн притисног суда4
- API стандарди: Термичка заштита процесне опреме
- OSHA прописи: Безбедност радника у термичким системима
- Прописи о заштити животне средине: Безбедно термичко испуштање
Стратегије усаглашености:
- Стандарди дизајна: Пратите признате кодове за термални дизајн
- Анализа безбедности: Извршите анализу топлотних опасности
- Документација: Водите евиденцију о термичкој безбедности
- Обука: Едуковати особље о топлотним опасностима
Процена и управљање ризицима
Компрехензивна процена ризика мора да обухвати ефекте топлотног притиска како би се идентификовали и ублажили потенцијални ризици.
Процес процене ризика:
- Идентификација опасности: Идентификовати изворе термичког притиска
- Анализа последица: Процените потенцијалне исходе
- Процена вероватноће: Одредите вероватноћу настанка
- Рангирање ризика: Дајте приоритет ризицима за ублажавање
- Стратегије ублажавања: Применити заштитне мере
Мере за ублажавање ризика:
- Дизајн маргина: Прекомерна опрема за термичке ефекте
- Вишак заштите: Више безбедносних система
- Превентивно одржавање: Редовно инспекцијско прегледање система
- Обука оператера: Свест о топлотној безбедности
- Планирање за ванредне ситуације: Поступци реаговања на термални инцидент
Како се закон о притиску интегрише са другим гасним законима?
Закон о притиску се интегрише са другим основним гасним законима како би се формирало свеобухватно разумевање понашања гаса, стварајући основу за напредну термодинамичку анализу.
Закон притиска се интегрише са Бојлевим законом (), Чарлсов закон (), и Авогадроов закон за формирање закона о мешаном гасу и једначине идеалног гаса , пружајући потпун опис понашања гаса.
Интеграција закона о мешаним гасовима
Закон о притиску се комбинује са другим гасним законима како би створио свеобухватан комбиновани гасни закон који описује понашање гаса када се више својстава истовремено мењају.
Комбиновани закон о гасовима:
Ова једначина обухвата:
- Закон о притиску: (константна запремина)
- Бојлов закон: (константна температура)
- Чарлсов закон: (постојан притисак)
Појединачна деривација права:
Према закону о мешавини гасова:
- Постави V₁ = V₂ → (Закон о притиску)
- Постави T₁ = T₂ → (Бојлов закон)
- Постави P₁ = P₂ → (Чарлсов закон)
Развој закона идеалног гаса
Закон притиска доприноси закону идеалног гаса, који пружа најсвеобухватнији опис понашања гаса.
Закон идеалног гаса:
Извеђење из гасних закона:
- Бојлов закон: P ∝ 1/V (константна T, n)
- Чарлсов закон: V ∝ T (константа P, n)
- Закон о притиску: (константна V, n)
- Авогадроов закон: V ∝ n (константа P, T)
Комбиновано: →
Интеграција термодинамичких процеса
Закон притиска се интегрише са термодинамичким процесима како би описао понашање гаса под различитим условима.
Типови процеса:
| Процес | Постојана својина | Примена закона о притиску |
|---|---|---|
| изохорични | Обим | Директна примена: |
| Изобаричан | Притисак | У комбинацији са Чарлсовим законом |
| Изотермални | Температура | Нема директне примене |
| Адијабатичан | Нема преноса топлоте | Модификовани односи |
Изохорични процес (константан волумен):
(директна примена закона)
Рад = 0 (без промене обима)
(топлота је једнака промени унутрашње енергије)
Интеграција понашања стварног гаса
Закон о притиску Простире се на понашање идеалног гаса кроз једначине стања које узимају у обзир молекуларне интеракције и ограничену величину молекула5.
Ван дер Ваалсова једначина:
Где:
- a = корекција интермолекуларне привлачности
- b = Корекција молекуларног обима
Закон о стварном притиску гаса:
Закон о притиску и даље важи, али са корекцијама за понашање идеалног гаса.
Интеграција кинетичке теорије
Закон о притиску се интегрише са кинетичко-молекуларном теоријом како би пружио микроскопско разумевање макроскопског понашања гаса.
Односи кинетичке теорије:
(микроскопски притисак)
(веза између брзине и температуре)
Стога: (закон притиска по кинетичкој теорији)
Предности интеграције:
- Микроскопско разумевање: Молекуларна основа за макроскопске законе
- Предвиђајућа способност: Предвиђање понашања из првих принципа
- Идентификација ограничења: Услови у којима закони не важе
- Напредне примене: Комплексна анализа система
Недавно сам сарађивао са јужнокорејским инжењером по имену Парк Мин-џун, чији је вишестепени систем компресије захтевао интегрисану анализу закона гасова. Правилном применом закона притиска у комбинацији са другим законима гасова оптимизовали смо дизајн система како бисмо постигли смањење енергије за 43%, уз побољшање перформанси за 67%.
Практичне примене интеграције
Интегрисане примене закона о гасу решавају сложене индустријске проблеме који укључују више променљивих и услова.
Проблеми са више променљивих:
- Синхроне промене P, V и T: Користите закон о мешавини гасова
- Оптимизација процеса: Применити одговарајуће комбинације закона
- Анализа безбедности: Размотрите све могуће промене променљивих
- Дизајн система: Интегришите ефекте вишегасног закона
Инжењерске примене:
- Дизајн компресора: Интегришите ефекте притиска и запремине
- Анализа топлотног разменљивача: Комбинујте топлотне и притисне ефекте
- Контрола процеса: Користите интегрисане односе за контролу
- Системи безбедностиУзети у обзир све интеракције по закону о гасовима.
Закључак
Закон притиска (Гај-Лусаков закон) утврђује да је притисак гаса директно пропорционалан апсолутној температури при константном обиму (), пружајући суштинско разумевање за пројектовање термичких система, анализу безбедности и контролу индустријских процеса у којима промене температуре утичу на услове притиска.
Често постављана питања о закону притиска у физици
Шта је закон притиска у физици?
Закон притиска, познат и као Геј-Лусаков закон, наводи да је притисак гаса директно пропорционалан његовој апсолутној температури када запремина и количина остају константне, изражено као P₁/T₁ = P₂/T₂ или P ∝ T.
Како се закон притиска односи на молекуларно понашање?
Закон о притиску одражава молекуларно-кинетичку теорију, по којој више температуре повећавају брзину молекула и интензитет судара са зидовима посуде, стварајући већи притисак кроз учесталије и снажније молекуларне ударе.
Које су математичке примене закона притиска?
Математичке примене обухватају израчунавање промена притиска у зависности од температуре (P₂ = P₁ × T₂/T₁), одређивање коефицијената притиска (β = 1/T) и пројектовање термичких безбедносних система са одговарајућим маргинама притиска.
Како се закон о притиску примењује на индустријску безбедност?
Примене у индустријској безбедности обухватају одређивање величине вентила за ослобађање притиска, заштиту од термичког пренапона, системе за праћење температуре и процедуре за хитне случајеве термичких догађаја који би могли изазвати опасно повећање притиска.
Која је разлика између закона притиска и других гасних закона?
Закон притиска повезује притисак са температуром при константном обиму, док Бојлов закон повезује притисак са обимом при константној температури, а Чарлсов закон повезује обиму са температуром при константном притиску.
Како се закон притиска интегрише са законом идеалног гаса?
Закон притиска се комбинује са другим гасним законима и формира једначину идеалног гаса PV = nRT, где је однос притиска и температуре (P ∝ T) једна од компоненти свеобухватног описа понашања гаса.
-
“Геј-Лусаков закон”,
https://en.wikipedia.org/wiki/Gay-Lussac%27s_law. Објашњава термодинамички принцип да се притисак мења пропорционално апсолутној температури при константном обиму. Улога доказа: механизам; Тип извора: истраживање. Потврђује: притисак гаса је директно пропорционалан његовој апсолутној температури. ↩ -
“Кинетичка теорија гасова”,
http://hyperphysics.phy-astr.gsu.edu/hbase/Kinetic/kinthe.html. Описује како се термална енергија претвара у молекуларну кинетичку енергију и учесталост судара. Доказ улоге: механизам; Тип извора: истраживање. Потврђује: пораст температуре повећава просечну молекуларну брзину, што доводи до чешћих и интензивнијих судара са зидом. ↩ -
“Максвелова-Болцманова дистрибуција”,
https://en.wikipedia.org/wiki/Maxwell%E2%80%93Boltzmann_distribution. Описује статистичку расподелу брзина честица у идеалним гасовима у термичкој равнотежи. Улога доказа: општа подршка; Тип извора: истраживање. Подржава: Промене температуре мењају Максвелово-Болцманову расподелу брзина. ↩ -
“BPVC одељак VIII – Правила за конструкцију притисних посуда,
https://www.asme.org/codes-standards/bpvc-standards. Стандард који утврђује инжењерске критеријуме за топлотне и притисачне оптерећења у пројектовању посуда. Улога доказа: општа подршка; Тип извора: стандард. Подржава: ASME Boiler Code: термички дизајн притисних посуда. ↩ -
“Једначина ван дер Ваалса”,
https://chem.libretexts.org/Bookshelves/Physical_and_Theoretical_Chemistry_Textbook_Maps/Supplemental_Modules_(Physical_and_Theoretical_Chemistry)/Physical_Properties_of_Matter/States_of_Matter/Gases/Non-Ideal_Gas_Behavior/The_van_der_Waals_Equation. Објашњава модификације закона идеалног гаса како би се узели у обзир стварни молекуларни волумени и међумолекуларне силе. Улога доказа: механизам; Тип извора: истраживање. Подржава: проширује се на понашање стварних гасова кроз једначине стања које узимају у обзир молекуларне интеракције и коначну величину молекула. ↩


