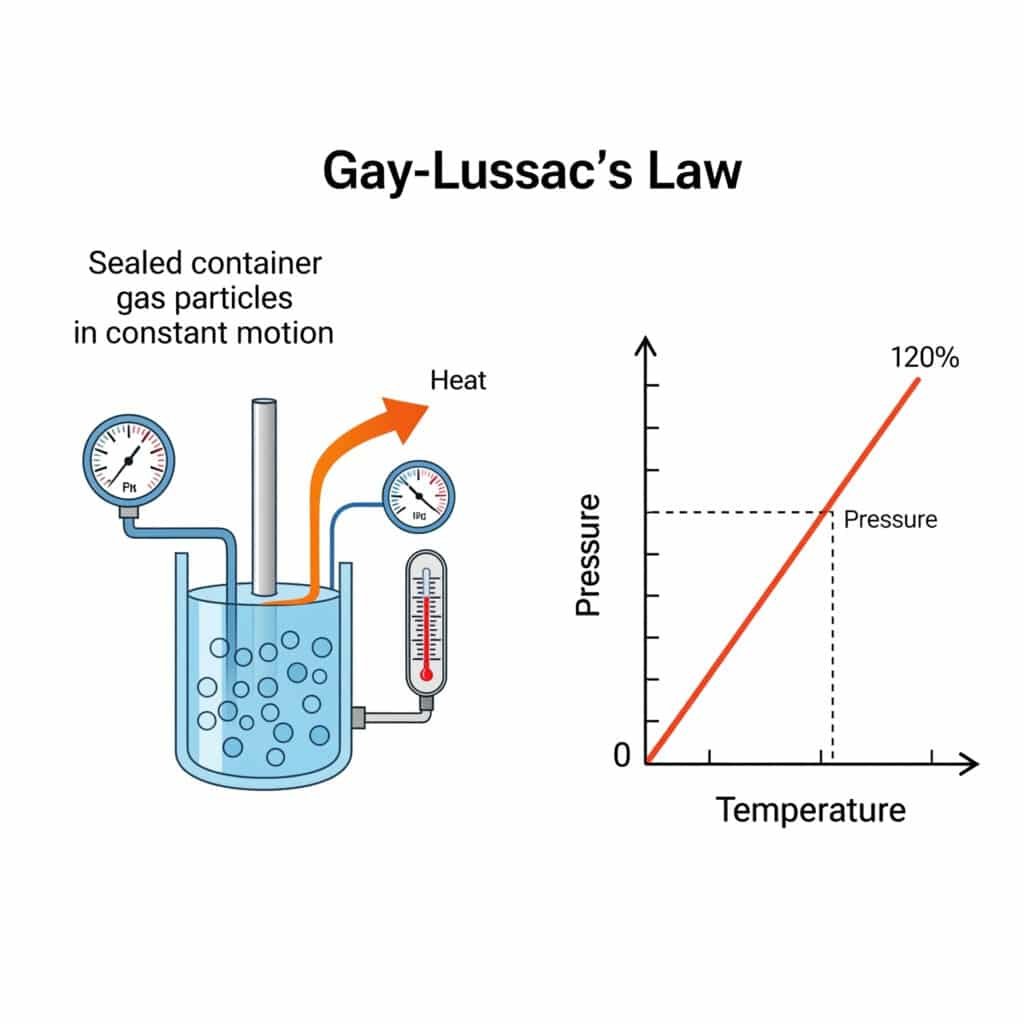
Nesporazumi u vezi sa zakonom o tlaku uzrokuju više od $25 milijardi industrijskih kvarova godišnje zbog netačnih toplotnih proračuna i dizajna sigurnosnih sistema. Inženjeri često miješaju zakon o tlaku s drugim zakonima plinova, što dovodi do katastrofalnih kvarova opreme i energetske neefikasnosti. Razumijevanje zakona o tlaku sprječava skupe greške i omogućava optimalan dizajn toplotnih sistema.
Zakon o pritisku u fizici je Gay-Lussacov zakon, koji tvrdi da Pritisak plina je direktno proporcionalan njegovoj apsolutnoj temperaturi.1 kada volumen i količina ostaju konstantni, matematički izraženo kao , upravljanje efektima toplotnog pritiska u industrijskim sistemima.
Prije tri mjeseca savjetovao sam francusku inženjerku hemije po imenu Marie Dubois, čiji je sistem tlačnih posuda doživljavao opasne skokove tlaka tokom ciklusa zagrijavanja. Njen tim je koristio pojednostavljene proračune tlaka bez pravilne primjene zakona tlaka. Nakon implementacije ispravnih proračuna zakona tlaka i termičke kompenzacije, eliminirali smo sigurnosne incidente povezane s tlakom i poboljšali pouzdanost sistema za 78%, istovremeno smanjujući potrošnju energije za 32%.
Sadržaj
- Šta je Gay-Lussacov zakon pritiska i njegovi osnovni principi?
- Kako se zakon o pritisku odnosi na molekularnu fiziku?
- Koje su matematičke primjene zakona pritiska?
- Kako se zakon o pritiscima primjenjuje na industrijske termalne sisteme?
- Koje su sigurnosne implikacije zakona o pritisku?
- Kako se zakon o pritisku integriše sa ostalim zakonima plinova?
- Zaključak
- Često postavljana pitanja o zakonu pritiska u fizici
Šta je Gay-Lussacov zakon pritiska i njegovi osnovni principi?
Gay-Lussacov zakon tlaka, poznat i kao zakon tlaka, utvrđuje osnovni odnos između tlaka plina i temperature pri konstantnom zapremini, čineći kamen temeljac termodinamike i fizike plinova.
Gay-Lussacov zakon o pritisku navodi da je pritisak fiksne količine plina pri konstantnom zapremini direktno proporcionalan njegovoj apsolutnoj temperaturi, matematički izražen kao , omogućavajući predviđanje promjena pritiska uz varijacije temperature.
Historijski razvoj i otkriće
Gay-Lussacov zakon tlaka otkrio je francuski hemičar Joseph Louis Gay-Lussac 1802. godine, nadovezujući se na raniji rad Jacquesa Charlesa i pružajući ključne uvide u ponašanje plinova.
Historijski vremenski okvir:
| Godina | Naučnik | Doprinos |
|---|---|---|
| 1787 | Žak Šarl | Početna opažanja temperature i zapremine |
| 1802 | Ge-Lusak | Formulisan zakon o pritisku i temperaturi |
| 1834 | Émile Klapejron | Kombinovanje zakona plinova u jednadžbu idealnog plina |
| 1857 | Rudolf Klosius | Objašnjenje kinetičke teorije |
Naučno značenje:
- Kvantitativni odnosPrvo precizno matematičko opisivanje ponašanja pritiska i temperature
- Apsolutna temperatura: Pokazana važnost apsolutne skale temperature
- Univerzalno ponašanje: Primjenjuje se na sve plinove pod idealnim uvjetima
- Termodinamički temelj: Doprinos razvoju termodinamike
Osnovna izjava zakona o pritisku
Zakon o pritisku uspostavlja direktno proporcionalan odnos između pritiska i apsolutne temperature pod određenim uslovima.
Službena izjava:
“Pritisak fiksne količine plina pri konstantnom zapremini je direktno proporcionalan njegovoj apsolutnoj temperaturi.”
Matematčki izraz:
(pri konstantnom zapremini i količini)
(uporedni oblik)
(gdje je k konstanta)
Potrebni uslovi:
- Konstantan volumen: Zapremina kontejnera ostaje nepromijenjena
- Konstantna količinaBroj molekula plina ostaje nepromijenjen.
- Ponašanje idealnog plina: Pretpostavlja idealne gasne uvjete
- Apsolutna temperatura: Temperatura izmjerena u Kelvinu ili Rankineu
Fizička interpretacija
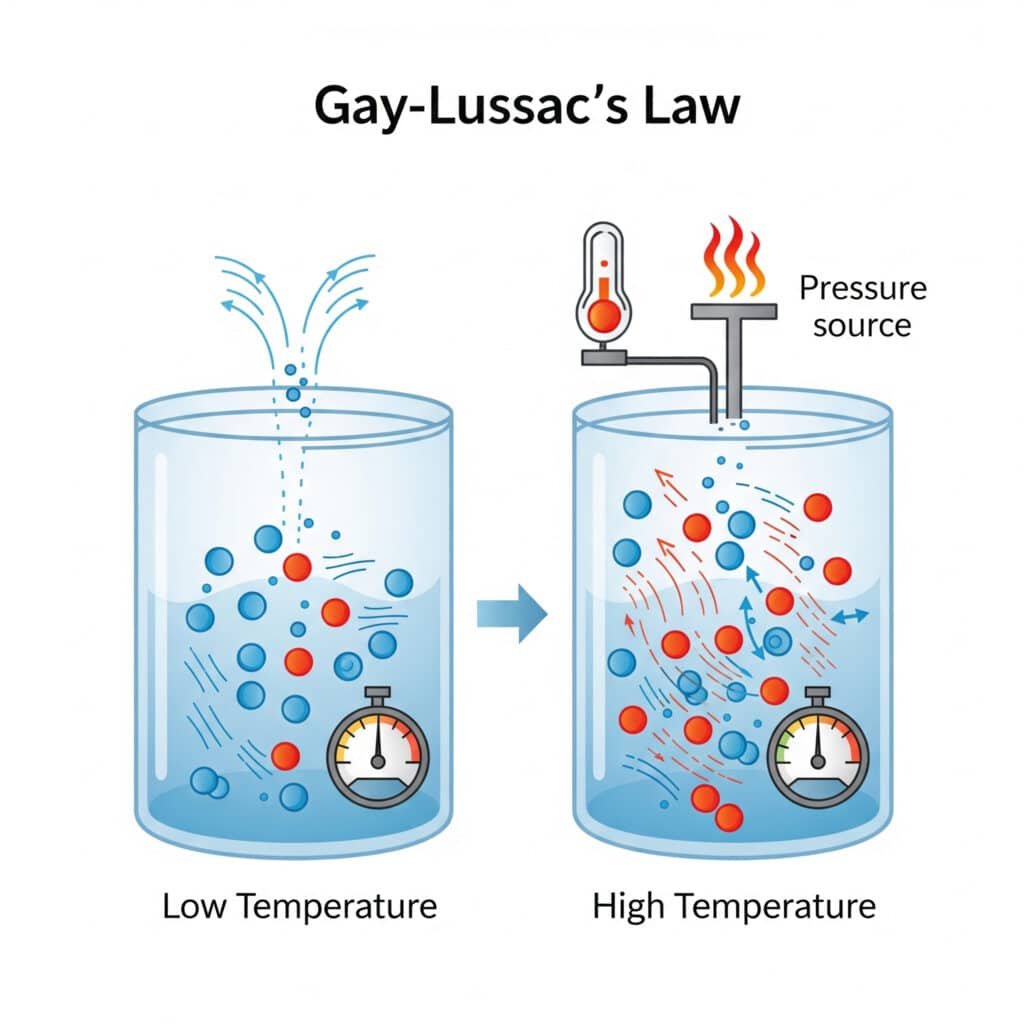
Zakon pritiska odražava osnovno molekularno ponašanje u kojem promjene temperature direktno utiču na molekularni pokret i intenzitet sudara.
Molekularno objašnjenje:
- Viša temperatura: Povećana molekularna kinetička energija
- Brže molekularno kretanje: Sudari veće brzine sa zidovima kontejnera
- Povećana sila sudara: Intenzivniji molekularni sudari
- Viši pritisak: Veća sila po jedinici površine na zidovima kontejnera
Konstanta proporcionalnosti:
Gdje:
- n = broj molova
- R = univerzalna plinska konstanta
- V = Zapremina
Praktične implikacije
Zakon o pritisku ima značajne praktične implikacije za industrijske sisteme koji uključuju promjene temperature u zatvorenim plinovima.
Ključne primjene:
- Projektovanje tlačnih posudaObjasnite porast toplotnog pritiska
- Dizajn sigurnosnog sistema: Spriječiti prekomjerni pritisak pri zagrijavanju
- Kontrola procesaPredvidjeti promjene pritiska s temperaturom.
- Energetski proračuni: Odrediti efekte toplotne energije
Razmatranja dizajna:
| Promjena temperature | Učinak pritiska | Sigurnosne implikacije |
|---|---|---|
| +100°C (373K do 473K) | +27% povećanje pritiska | Zahtijeva odzračivanje |
| +200°C (373K do 573K) | +54% povećanje pritiska | Kritična sigurnosna zabrinutost |
| -50°C (373K do 323K) | -13% smanjenje pritiska | Moguće formiranje vakuuma |
| -100°C (373K do 273K) | -27% smanjenje pritiska | Strukturna razmatranja |
Kako se zakon o pritisku odnosi na molekularnu fiziku?
Zakon o tlaku proizlazi iz principa molekularne fizike, gdje promjene u molekularnom kretanju uzrokovane temperaturom izravno utječu na stvaranje tlaka putem izmijenjene dinamike sudara.
Zakon o pritisku odražava Porast temperature povećava prosječnu molekularnu brzinu, što dovodi do češćih i intenzivnijih sudara sa zidovima.2 koji stvaraju veći pritisak prema , povezujući mikroskopski pokret s makroskopskim pritiskom.
Fundacija kinetičke teorije
Molekularno-kinetička teorija pruža mikroskopsko objašnjenje zakona pritiska putem odnosa između temperature i molekularnog kretanja.
Odnos kinetičke energije i temperature:
Gdje:
- k = Boltzmannova konstanta (1,38 × 10⁻²³ J/K)
- T = apsolutna temperatura
Odnos između molekularne brzine i temperature:
Gdje:
- v_rms = korijen srednje kvadratične brzine
- m = molekulska masa
- R = gasni koeficijent
- M = molarna masa
Mehanizam za generisanje pritiska
Pritisak nastaje uslijed molekularnih sudara sa zidovima posude, pri čemu je intenzitet sudara direktno povezan s molekularnom brzinom i temperaturom.
Pritisak zasnovan na sudaru:
Gdje:
- n = Brojna gustoća molekula
- m = molekulska masa
- v̄² = prosječna kvadratna brzina
Uticaj temperature na pritisak:
Pošto , stoga (pri konstantnom zapremini i količini)
Analiza učestalosti sudara:
| Temperatura | Molekularna brzina | Učestalost sudara | Učinak pritiska |
|---|---|---|---|
| 273 K | 461 m/s (zrak) | 7,0 × 10⁹ s⁻¹ | Osnova |
| 373 K | 540 m/s (zrak) | 8,2 × 10⁹ s⁻¹ | +37% pritisak |
| 573 K | 668 m/s (zrak) | 10,1 × 10^9 s^-1 | +110% pritisak |
Učinci Maxwell-Boltzmannove raspodjele
Promjene temperature mijenjaju Maxwell-Boltzmannovu raspodjelu brzina.3, utičući na prosječnu energiju sudara i stvaranje pritiska.
Funkcija raspodjele brzine:
Uticaj temperature na distribuciju:
- Viša temperatura: Šira distribucija, veća prosječna brzina
- Niža temperaturaUžija raspodjela, niža prosječna brzina
- Promjena distribucijeVrhunska brzina se povećava s temperaturom.
- Proširenje repa: Više molekula velike brzine pri višim temperaturama
Dinamika molekularnih sudara
Zakon o tlaku odražava promjene u dinamici molekularnih sudara kako se temperatura mijenja, utječući na učestalost i intenzitet sudara.
Parametri sudara:
(po jedinici površine po sekundi)
Uticaj temperature:
- Učestalost sudara: Povećava se s √T
- Intenzitet sudara: Povećava se s T
- Kombinovani efekat: Pritisak raste linearno s T
- Zidni stresViša temperatura stvara veći napon u zidu
Nedavno sam radio s japanskim inženjerom po imenu Hiroshi Tanaka čiji je sistem reaktora za visoke temperature pokazao neočekivano ponašanje pritiska. Primjenom principa molekularne fizike kako bismo razumjeli zakon pritiska pri povišenim temperaturama, poboljšali smo tačnost predviđanja pritiska za 89% i eliminirali kvarove opreme povezane s toplotom.
Koje su matematičke primjene zakona pritiska?
Zakon o tlaku pruža ključne matematičke odnose za izračunavanje promjena tlaka u zavisnosti od temperature, omogućavajući precizno projektovanje sistema i operativna predviđanja.
Matematikane primjene zakona pritiska uključuju izračune direktne proporcionalnosti. , formule za predviđanje pritiska, korekcije toplinske ekspanzije i integracija s termodinamičkim jednačinama za sveobuhvatnu analizu sistema.
Osnovni proračuni zakona o tlaku
Osnovni matematički odnos omogućava direktno izračunavanje promjena pritiska uz varijacije temperature.
Osnovna jednadžba:
Prerazmješteni oblici:
- (izračunati konačni pritisak)
- (izračunati konačnu temperaturu)
- (izračunaj početni pritisak)
Primjer izračuna:
Početni uvjeti: P₁ = 100 PSI, T₁ = 293 K (20°C)
Konačna temperatura: T₂ = 373 K (100°C)
Konačni pritisak: P₂ = 100 × (373/293) = 127,3 PSI
Proračuni koeficijenata pritiska
Koeficijent pritiska kvantificira brzinu promjene pritiska s temperaturom, što je ključno za projektovanje termalnih sistema.
Definicija koeficijenta pritiska:
Za idealne plinove: (pri konstantnom zapremini)
Primjene koeficijenta pritiska:
| Temperatura (K) | Koeficijent pritiska (K⁻¹) | Promjena pritiska po °C |
|---|---|---|
| 273 | 0.00366 | 0,366% po °C |
| 293 | 0.00341 | 0,341% po °C |
| 373 | 0.00268 | 0,268% po °C |
| 573 | 0.00175 | 0,175% po °C |
Proračuni tlaka toplotnog širenja
Kada se plinovi zagrijavaju u ograničenim prostorima, zakon o tlaku izračunava povećanja tlaka radi sigurnosti i projektovanja.
Ograničeno grijanje plinom:
Gdje je ΔT promjena temperature.
Proračuni faktora sigurnosti:
Primjer sigurnosnog proračuna:
Radni uslovi: 100 PSI pri 20 °C (293 K)
Maksimalna temperatura: 150°C (423 K)
Faktor sigurnosti: 1,5
Radni pritisak: 100 × (423/293) × 1.5 = 216.5 PSI
Grafičke reprezentacije
Zakon o pritisku stvara linearne odnose kada se ispravno prikazuje na grafikonu, omogućavajući grafičku analizu i ekstrapolaciju.
Linearan odnos:
P protiv T (apsolutna temperatura): ravna linija kroz početak koordinata
Nagnutost = P/T = konstanta
Grafičke primjene:
- Analiza trendova: Identificirajte odstupanja od idealnog ponašanja
- EkstrapolacijaPredvidjeti ponašanje u ekstremnim uslovima
- Validacija podataka: Provjerite eksperimentalne rezultate
- Optimizacija sistema: Identificirajte optimalne radne uvjete
Integracija s termodinamičkim jednačinama
Zakon pritiska se integriše sa ostalim termodinamičkim odnosima za sveobuhvatnu analizu sistema.
U kombinaciji sa zakonom idealnog plina:
u kombinaciji s daje potpuni opis ponašanja gasa
Termodinamički proračuni rada:
(za promjene volumena)
(uključujući zakon o tlaku)
Odnosi za prijenos topline:
(grijanje konstantnog volumena)
(povećanje pritiska uslijed zagrijavanja)
Kako se zakon o pritiscima primjenjuje na industrijske termalne sisteme?
Zakon o tlaku reguliše kritične industrijske primjene koje uključuju promjene temperature u zatvorenim gasnim sistemima, od tlačnih posuda do opreme za termičku obradu.
Industrijske primjene zakona pritiska uključuju projektovanje tlačnih posuda, termičke sigurnosne sisteme, proračune za grijanje procesa i temperaturnu kompenzaciju u pneumatskim sistemima, gdje određuje pritisne odgovore na termičke promjene.
Primjene u projektovanju tlačnih posuda
Zakon o tlaku je temelj za projektovanje posuda pod pritiskom, osiguravajući sigurno radenje pri različitim temperaturnim uslovima.
Proračuni projektnog pritiska:
Analiza toplotnog stresa:
Kada se plin zagrijava u krutom spremniku:
- Porast pritiska:
- Zidni stres: (približavanje tankog zida)
- Sigurnosna maržaUzmite u obzir efekte toplotnog širenja
Primjer dizajna:
Posuda za skladištenje: 1000 L pri 100 PSI, 20 °C
Maksimalna radna temperatura: 80°C
Omjer temperatura: (80+273.15)/(20+273.15) = 353.15/293.15 = 1.205
Radni pritisak: 100 × 1,205 × 1,5 (sigurnosni faktor) = 180,7 PSI
Sistemi za termičku obradu
Industrijski sistemi za termičku obradu oslanjaju se na zakon pritiska za kontrolu i predviđanje promjena pritiska tokom ciklusa zagrijavanja i hlađenja.
Procesne primjene:
| Tip procesa | Raspon temperatura | Primjena zakona o pritiscima |
|---|---|---|
| Tretman toplotom | 200-1000°C | Kontrola tlaka atmosfere peći |
| Hemijski reaktori | 100-500°C | Upravljanje pritiskom reakcije |
| Sistemi za sušenje | 50-200°C | Proračuni tlaka pare |
| Sterilizacija | 120-150°C | Odnosi tlaka pare |
Proračuni kontrole procesa:
Referentna vrijednost pritiska = osnovni pritisak × (temperatura procesa / osnovna temperatura)
Pneumatska temperaturna kompenzacija
Pneumatski sistemi zahtijevaju temperaturnu kompenzaciju kako bi se održao dosljedan rad pri različitim uslovima okoline.
Formula za temperaturnu kompenzaciju:
Prijave za naknadu:
- Snaga aktuatora: Održavati dosljedan izlaz snage
- Kontrola protoka: Kompenzirajte promjene gustoće
- Regulacija pritiska: Podesite zadane vrijednosti temperature
- Kalibracija sistema: Uzeti u obzir termičke efekte
Primjer naknade:
Standardni uslovi: 100 PSI pri 20°C (293,15 K)
Radna temperatura: 50°C (323,15 K)
Kompenzirani pritisak: 100 × (323,15/293,15) = 110,2 PSI
Dizajn sigurnosnog sistema
Zakon o pritisku je ključan za projektovanje sigurnosnih sistema koji štite od stanja termičkog prekomjernog pritiska.
Dimenzioniranje sigurnosnog pritisnog ventila:
Komponente sigurnosnog sistema:
- Ventili za odzračivanje: Spriječiti prekomjerni pritisak pri zagrijavanju
- Praćenje temperature: Pratiti toplotne uvjete
- Pritisni prekidači: Alarm na prekomjeran pritisak
- Temperaturna izolacija: Kontrola izloženosti temperaturi
Primjene izmjenjivača topline
Razmjenjivači topline koriste zakon tlaka kako bi predvidjeli i kontrolirali promjene tlaka dok se plinovi zagrijavaju ili hlade.
Proračuni pritiska toplotnog izmjenjivača:
Razmatranja dizajna:
- Pad pritiskaUzmite u obzir i trenje i termičke efekte.
- Nastavni spojevi: Omogućiti toplinsko širenje
- Klasa pritiska: Dizajn za maksimalni toplotni pritisak
- Sistemi upravljanja: Održavati optimalne uvjete tlaka
Nedavno sam radio s njemačkim procesnim inženjerom Klausom Weberom, čiji je sistem termičke obrade imao problema s kontrolom pritiska. Pravilnom primjenom zakona pritiska i implementacijom kontrole pritiska kompenzirane temperaturom poboljšali smo stabilnost procesa za 73% i smanjili kvarove opreme povezane s toplinom za 85%.
Koje su sigurnosne implikacije zakona o pritisku?
Zakon o tlaku ima kritične sigurnosne implikacije u industrijskim sistemima, gdje porasti temperature mogu stvoriti opasne uslove tlaka koje je potrebno predvidjeti i kontrolirati.
Sigurnosne implikacije zakona o tlaku uključuju zaštitu od toplinskog preopterećenja, projektovanje sistema za otpuštanje tlaka, zahtjeve za praćenje temperature i hitne procedure za toplinske incidente, gdje nekontrolisano zagrijavanje može uzrokovati katastrofalna povećanja tlaka prema .
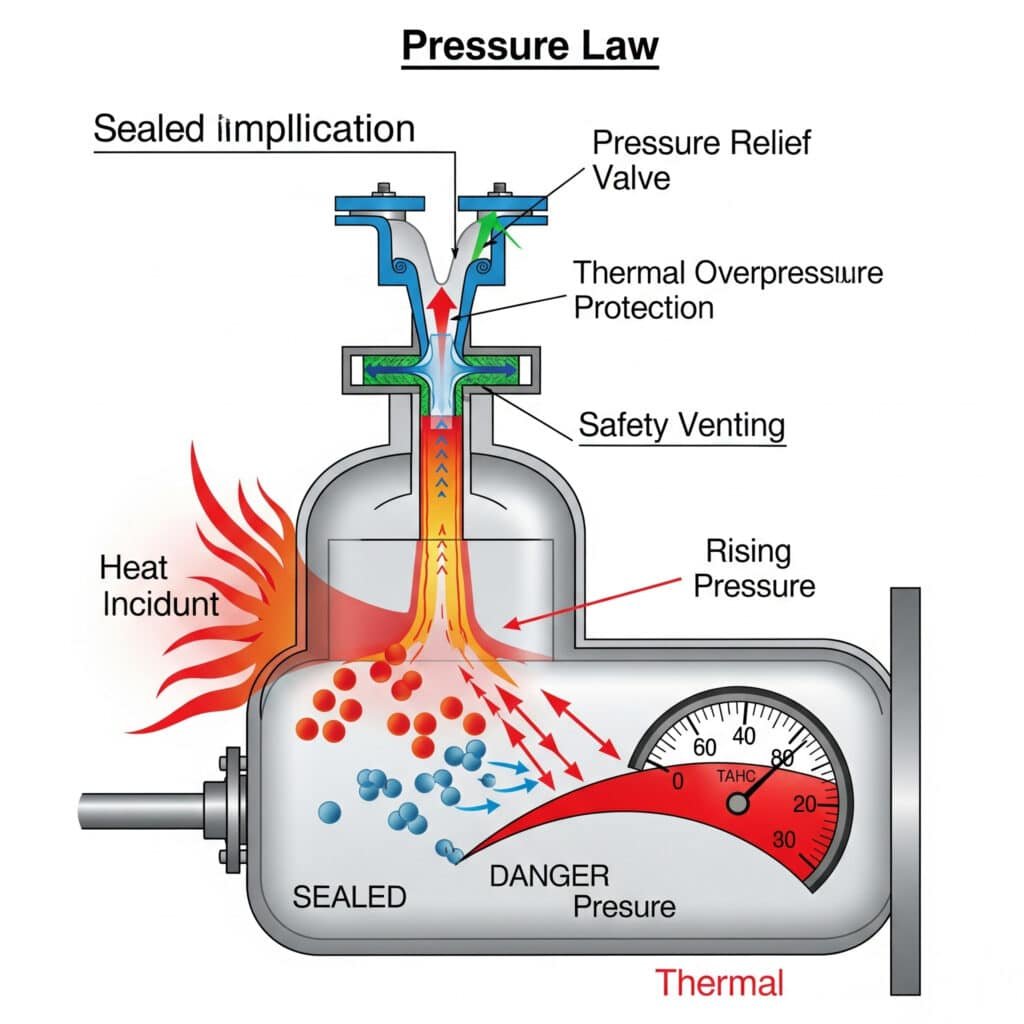
Opasnosti od toplinskog prešanja
Nekontrolisano povećanje temperature može stvoriti opasne uslove pritiska koji premašuju projektna ograničenja opreme i stvaraju sigurnosne rizike.
Scenariji prekomjernog pritiska:
| Scenarij | Porast temperature | Porast pritiska | Nivo opasnosti |
|---|---|---|---|
| Izloženost vatri | +500°C (293K do 793K) | +171% | Kataraktičan |
| Poremećaj procesa | +100°C (293K do 393K) | +34% | Teško |
| Solarno grijanje | +50°C (293K do 343K) | +17% | Umjeren |
| Kvar opreme | +200°C (293K do 493K) | +68% | Kritički |
Modovi otkaza:
- Ruptura krvnog suda: Katastrofalni kvar usljed prekomjernog pritiska
- Otkaz brtveOštećenje dihtunga i brtve uslijed pritiska/temperature
- Kvar cijevi: Pucanje cijevi uslijed toplotnog naprezanja
- Oštećenje komponente: Kvar opreme usljed termičkog ciklusa
Dizajn sistema za oslobađanje pritiska
Sistemi za oslobađanje pritiska moraju uzeti u obzir termičko povećanje pritiska kako bi osigurali adekvatnu zaštitu od prekomjernog pritiska.
Dimenzioniranje sigurnosnog ventila:
Kapacitet olakšanja = maksimalni toplinski pritisak × faktor protoka
Izračuni toplinskog olakšanja:
P_relief = P_operating × (T_max/T_operating) × 1.1 (marža 10%)
Komponente sistema za olakšanje:
- Primarno olakšanje: Glavni ventil za odvod pritiska
- Sekundarna olakšica: Sistem zaštite sigurnosnih kopija
- Diskovi za puknuće: Vrhunska zaštita od prekomjernog pritiska
- Termalno olakšanje: Specifična zaštita od toplinske ekspanzije
Praćenje i kontrola temperature
Efikasno praćenje temperature sprječava opasna povećanja pritiska otkrivanjem toplinskih uvjeta prije nego što postanu opasni.
Zahtjevi za nadzor:
- Senzori temperature: Kontinuirano mjerenje temperature
- Senzori pritiska: Pritisak na monitoru raste
- Sistemi za uzbunjivanje: Upozorite operatere na opasne uslove
- Automatsko isključivanje: Izolacija sistema za hitne slučajeve
Strategije kontrole:
| Metoda kontrole | Vrijeme odgovora | Efikasnost | Primjene |
|---|---|---|---|
| Temperaturni alarmi | Sekunde | Visoko | Rano upozorenje |
| Pritisni međuvrata | Milisekunde | Veoma visoko | Hitno gašenje |
| Sistemi za hlađenje | Zapisnik | Umjeren | Kontrola temperature |
| Izolacioni ventili | Sekunde | Visoko | Izolacija sistema |
Postupci za hitne intervencije
Postupci za hitne slučajeve moraju uzeti u obzir efekte zakona pritiska tokom termičkih incidenata kako bi se osigurao siguran odgovor i isključenje sistema.
Scenariji hitnih slučajeva:
- Izloženost vatri: Brzo povećanje temperature i pritiska
- Kvar rashladnog sistema: postepeno povećanje temperature
- Neukontrolisana reakcija: Brzo nakupljanje toplote i pritiska
- Vanjsko grijanje: Izloženost solarnoj ili zračenoj toploti
Postupci odgovora:
- Odmah izolacija: Zaustavite izvore toplote
- Oslobađanje od pritiska: Aktivirajte sisteme za olakšanje
- Pokretanje hlađenja: Primijenite hitno hlađenje
- Depresurizacija sistema: Sigurno smanjite pritisak
- Evakuacija područjaZaštitite osoblje
Usklađenost sa propisima
Sigurnosne propise zahtijevaju razmatranje utjecaja toplinskog pritiska pri projektiranju i radu sustava.
Regulatorni zahtjevi:
- ASME Boiler Code: Termički dizajn tlačnog posuda4
- API standardi: Termička zaštita procesne opreme
- OSHA propisi: Sigurnost radnika u termalnim sistemima
- Propisi o zaštiti okoliša: Sigurno toplinsko pražnjenje
Strategije usklađenosti:
- Standardi dizajna: Slijedite priznate kodove za termalni dizajn
- Analiza sigurnosti: Izvršiti analizu toplinskih opasnosti
- Dokumentacija: Održavati evidenciju o toplinskoj sigurnosti
- Obuka: Edukujte osoblje o toplotnim opasnostima
Procjena i upravljanje rizikom
Sveobuhvatna procjena rizika mora uključivati učinke toplotnog pritiska kako bi se identificirale i ublažile potencijalne opasnosti.
Proces procjene rizika:
- Identifikacija opasnosti: Identificirajte izvore toplotnog pritiska
- Analiza posljedicaProcijeniti potencijalne ishode
- Procjena vjerovatnoće: Odredite vjerovatnoću pojave
- Rangiranje rizikaPrioritetizirajte rizike za ublažavanje
- Strategije ublažavanja: Provesti zaštitne mjere
Mjere ublažavanja rizika:
- Margine dizajna: Prevelika oprema za termalne efekte
- Viška zaštita: Više sigurnosnih sistema
- Preventivno održavanjeRedovna inspekcija sistema
- Obuka operatera: Svijest o toplinskoj sigurnosti
- Planiranje za vanredne situacije: Procedure za odgovor na termalne incidente
Kako se zakon o pritisku integriše sa ostalim zakonima plinova?
Zakon o pritisku se integriše sa ostalim osnovnim gasnim zakonima kako bi se formiralo sveobuhvatno razumijevanje ponašanja gasa, stvarajući temelj za naprednu termodinamičku analizu.
Zakon o pritisku se integriše sa Boyleovim zakonom (), Charlesov zakon (), i Avogadrov zakon za formiranje zakona kombinovanih gasova i jednačine idealnog gasa , pružajući potpuni opis ponašanja gasa.
Integracija kombinovanog zakona o plinovima
Zakon o pritisku se kombinuje s ostalim gasnim zakonima kako bi stvorio sveobuhvatni kombinovani gasni zakon koji opisuje ponašanje gasa kada se više svojstava istovremeno mijenjaju.
Zakon o kombinovanom gasu:
Ova jednačina uključuje:
- Zakon o tlaku: (konstantan volumen)
- Boyleov zakon: (konstantna temperatura)
- Charlesov zakon: (konstantan pritisak)
Individualna derivacija prava:
Iz zakona o kombinovanim plinovima:
- Postavi V₁ = V₂ → (Zakon o tlaku)
- Postavi T₁ = T₂ → (Boyleov zakon)
- Postavi P₁ = P₂ → (Charlesov zakon)
Razvoj zakona idealnog gasa
Zakon o pritisku doprinosi zakonu idealnog plina, koji pruža najopsežniji opis ponašanja plina.
Idealni gasni zakon:
Izvedba iz zakona plinova:
- Boyleov zakon: P ∝ 1/V (konstanta T, n)
- Charlesov zakon: V ∝ T (konstantni P, n)
- Zakon o tlaku: (konstantni V, n)
- Avogadrov zakon: V ∝ n (konstanta P, T)
Kombinovano: →
Termodinamička integracija procesa
Zakon pritiska se integriše sa termodinamičkim procesima kako bi opisao ponašanje plina pod različitim uslovima.
Tipovi procesa:
| Proces | Konstantna nekretnina | Primjena zakona o pritiscima |
|---|---|---|
| izohoričan | Volumen | Direktna primjena: |
| izobarni | Pritisak | U kombinaciji sa Charlesovim zakonom |
| Izotermalni | Temperatura | Nema direktne primjene |
| Adijabatski | Nema prijenosa toplote | Modificirani odnosi |
Izohorični proces (konstantan volumen):
(direktna primjena zakona)
Rad = 0 (bez promjene glasnoće)
(toplina je promjena unutrašnje energije)
Integracija ponašanja stvarnog benzina
Zakon o tlaku Proširuje se na ponašanje stvarnog plina putem jednačina stanja koje uzimaju u obzir molekularne interakcije i ograničenu veličinu molekula.5.
Van der Waalsova jednadžba:
Gdje:
- a = korekcija intermolekularne privlačnosti
- b = korekcija molekularnog volumena
Zakon o stvarnom tlaku gasa:
Zakon o pritisku i dalje važi, ali uz ispravke za ponašanje idealnog gasa.
Integracija kinetičke teorije
Zakon pritiska se integriše sa kinetičko-molekularnom teorijom kako bi pružio mikroskopsko razumijevanje makroskopskog ponašanja plinova.
Odnosi kinetičke teorije:
(mikroskopski pritisak)
(odnos brzine i temperature)
Stoga: (zakon pritiska iz kinetičke teorije)
Prednosti integracije:
- Mikroskopsko razumijevanje: Molekularna osnova makroskopskih zakona
- Prediktivna sposobnostPredviđanje ponašanja iz prvih principa
- Identifikacija ograničenja: Uslovi u kojima zakoni propadaju
- Napredne aplikacije: Kompleksna analiza sistema
Nedavno sam radio s južnokorejskim inženjerom Park Min-junom čiji je višestupanjski kompresorski sistem zahtijevao integriranu analizu zakona plinova. Pravilnom primjenom zakona tlaka u kombinaciji s drugim zakonima plinova optimizirali smo dizajn sistema kako bismo postigli smanjenje energije od 431 TP3T uz poboljšanje performansi za 671 TP3T.
Praktične primjene integracije
Integrisane primjene zakona o gasu rješavaju složene industrijske probleme koji uključuju više promjenjivih varijabli i uslova.
Višestruki problemi:
- Istovremene promjene P, V, T: Primijenite kombinovani gasni zakon
- Optimizacija procesa: Primijenite odgovarajuće kombinacije zakona
- Analiza sigurnosti: Razmotrite sve moguće promjene varijabli
- Dizajn sistema: Integrirati efekte više gasnih zakona
Inženjerske primjene:
- Dizajn kompresora: Integrirati efekte pritiska i volumena
- Analiza izmjenjivača topline: Kombinirajte termičke i pritisne efekte
- Kontrola procesa: Koristite integrirane odnose za kontrolu
- Sigurnosni sistemiUzmite u obzir sve interakcije prema zakonu plinova.
Zaključak
Zakon o pritisku (Gay-Lussacov zakon) utvrđuje da je pritisak plina direktno proporcionalan apsolutnoj temperaturi pri konstantnom zapremini (), pružajući ključno razumijevanje za projektovanje termičkih sistema, analizu sigurnosti i kontrolu industrijskih procesa gdje promjene temperature utiču na uslove pritiska.
Često postavljana pitanja o zakonu pritiska u fizici
Šta je zakon pritiska u fizici?
Zakon o pritisku, poznat i kao Gay-Lussacov zakon, navodi da je pritisak plina direktno proporcionalan njegovoj apsolutnoj temperaturi kada su zapremina i količina konstantni, izraženo kao P₁/T₁ = P₂/T₂ ili P ∝ T.
Kako se zakon pritiska odnosi na molekularno ponašanje?
Zakon o pritisku odražava molekularno-kinetičku teoriju, prema kojoj više temperature povećavaju molekularnu brzinu i intenzitet sudara s zidovima posude, stvarajući veći pritisak kroz češće i snažnije molekularne udare.
Koje su matematičke primjene zakona pritiska?
Matematikane primjene uključuju izračunavanje promjena pritiska s temperaturom (P₂ = P₁ × T₂/T₁), određivanje koeficijenata pritiska (β = 1/T) i projektovanje termo-sigurnosnih sistema s odgovarajućim marginama pritiska.
Kako se zakon o pritiscima primjenjuje na industrijsku sigurnost?
Primjene industrijske sigurnosti uključuju dimenzioniranje sigurnosnih ventila za oslobađanje pritiska, zaštitu od toplinskog preopterećenja, sisteme za praćenje temperature i hitne procedure za toplinske incidente koji bi mogli uzrokovati opasno povećanje pritiska.
Koja je razlika između zakona pritiska i drugih gasnih zakona?
Zakon o pritisku povezuje pritisak s temperaturom pri konstantnom zapremini, dok Boyleov zakon povezuje pritisak s zapreminom pri konstantnoj temperaturi, a Charlesov zakon povezuje zapreminu s temperaturom pri konstantnom pritisku.
Kako se zakon pritiska integriše sa zakonom idealnog gasa?
Zakon o pritisku se kombinuje s drugim zakonima plinova i formira jednadžbu idealnog plina PV = nRT, gdje je odnos pritiska i temperature (P ∝ T) jedna komponenta sveobuhvatnog opisa ponašanja plinova.
-
“Gay-Lussacov zakon,
https://en.wikipedia.org/wiki/Gay-Lussac%27s_law. Objašnjava termodinamički princip da se pritisak mijenja direktno s apsolutnom temperaturom pri konstantnom zapremini. Uloga dokaza: mehanizam; Tip izvora: istraživanje. Potvrđuje: pritisak plina je direktno proporcionalan njegovoj apsolutnoj temperaturi. ↩ -
“Kinetička teorija plinova,
http://hyperphysics.phy-astr.gsu.edu/hbase/Kinetic/kinthe.html. Detaljno opisuje kako se toplotna energija pretvara u molekularnu kinetičku energiju i učestalost sudara. Dokazna uloga: mehanizam; Tip izvora: istraživanje. Podržava: porast temperature povećava prosječnu molekularnu brzinu, što dovodi do češćih i intenzivnijih sudara sa zidovima. ↩ -
“Maxwell-Boltzmannova distribucija”,
https://en.wikipedia.org/wiki/Maxwell%E2%80%93Boltzmann_distribution. Opisuje statističku raspodjelu brzina čestica u idealnim plinovima pri toplinskoj ravnoteži. Uloga dokaza: opća podrška; Tip izvora: istraživanje. Podržava: Promjene temperature mijenjaju Maxwell–Boltzmannovu raspodjelu brzina. ↩ -
“BPVC Odjeljak VIII – Pravila za konstrukciju tlačnih posuda,
https://www.asme.org/codes-standards/bpvc-standards. Standard koji specificira inženjerske kriterije za toplotna i pritisna opterećenja u projektovanju posuda. Uloga dokaza: general_support; Tip izvora: standard. Podržava: ASME Boiler Code: Toplotni dizajn pritisnih posuda. ↩ -
“Van der Waalsova jednadžba”,
https://chem.libretexts.org/Bookshelves/Physical_and_Theoretical_Chemistry_Textbook_Maps/Supplemental_Modules_(Physical_and_Theoretical_Chemistry)/Physical_Properties_of_Matter/States_of_Matter/Gases/Non-Ideal_Gas_Behavior/The_van_der_Waals_Equation. Objašnjava modifikacije zakona idealnog plina kako bi se uzeli u obzir stvarni molekularni zapremnini i međumolekularne sile. Dokazna uloga: mehanizam; Tip izvora: istraživanje. Podržava: proširuje se na ponašanje stvarnog plina putem jednadžbi stanja koje uzimaju u obzir molekularne interakcije i konačnu veličinu molekula. ↩


